Metastatik Prostat Kanserlerine Genel Bakış ve Metastatik Hormona Duyarlı Prostat Kanserlerinde Lokal Tedavi

-Metastatik prostat kanserleri “görüntüleme gereçlerinde metastaz tespit edilen prostat kanserleri” dir. Metastatik Pca’leri literatürde bazen “ileri evre prostat kanserleri” olarak da anılmaktadır. “The Advanced Prostate Cancer Consensus Conference 2019” raporlarında ileri evre prostat kanserleri “ lokal ileri evre prostat kanserlerinden başlayarak lokal tedaviden sonra biyokimyasal nüks (BCR) gelişenler, oligometastatik ve metastatik hormona duyarlı prostat kanserleri(mHSPC’leri), metastatik olmayan (M0) kastrasyon rezistant Pca’leri (CRPC), metastatik CRPC’leri(mCRPC)” olmak üzere geniş bir gurubu kapsamaktadır(1). Bu sebeple metastatik prostat kanserleri için “ileri evre prostat kanserleri” tanımı tam uyuşmamaktadır. AUA/ASTRO/SUO guideline’larında ise ileri evre prostat kanserleri “metastatik olmayan biyokimyasal nükslü kanserler ve metastatik hormona duyarlı kanserler” olarak iki gurupta ele alınmaktadır(2,3).
-Metastatik hormona duyarlı prostat kanserleri Türkçe ve İngilizce literatürde “metastatik hormon tedavisi görmemiş, hormona duyarlı, kastre olmamış, castration sensitive, castration naive, noncastre prostatic cancer” olarak birçok farklı terimlerle anılmaktadır.
Prostat kanseri için PSA taramalarının metastatik prostat kanseri insidansına ve prostat kanseri sebebiyle ölümlere (canser specific mortality, CSM) etkisi
-PSA tarama çalışmalarının primer amacı prostat kanserini (Pca) lokalize safhada tespit edebilmektir. Lokalize safhada tespit edildikten sonra bunların klinik önemli yada klinik önemsiz olma durumuna göre tedavi stratejileri belirlenmektedir. PSA ile tarama çalışmaları sonucunda tarama yapılan gurupta tarama yapılmayan popülasyona göre genel olarak daha çok lokalize prostat kanseri teşhis edilmektedir, aynı zamanda PSA taramaları ile tarama yapılmayan popülasyona göre metastatik prostat kanseri oranı düşük oranda bulunmakta ve PSA taramalarının “uzun sürede Pca sebebiyle ölümlerin tarama yapılmayanlara göre” azalmasını sağladığı belirmektedir(4-11). Ancak PSA taramalarının “overdiagnosis and overtreatment” riski yarattığı da kabul edilmektedir. Günümüzde taramaların yarattığı overdiagnozis riski multiparametrik MRI (mpMRI) kullanılarak yapılan biyopsi kararları ile azaltılabilmektedir.
-2012 de the US Preventive Services Task Force (USPSTF) rutin PSA taramalarını önermediğini belirterek PSA taramalarına sınırlama getirmiştir(12). Bunun sonucunda ABD’de lokalize Pca teşhis oranı azalırken metastatik Pca teşhis oranının arttığı, Pca sebebiyle mortalite oranının arttığı görülmüştür(13-17). Bu sonuca bağlı olarak USPSTF 2012 kararlarını 2018 de revize etmiştir; Pca için PSA taramalarının 55-69 yaş gurubunda yararlı olduğunu belirtmiştir(18,19).
-Prostat kanseri insidensinin ve prostat kanseri sebebiyle ölümün yaş artışına paralel arttığı bilinmektedir. Ancak PSA taramalarına hangi yaşta başlanması konusu netleşmemiştir, bu konuda tam bir konsensus bulunmamaktadır. EAU PSA testi yapılmasına 40-50 yaşlarında başlanmasını önerirken (20), Memorial Sloan Ketting Cancer Center (MSCC) ve National Comprehensive Cancer Network (NCCN) 45 yaşında başlanmasını (21,22), American Cancer Society (ACS) ve American College of Physicians 50 yaşında başlanmasını (23,24), US Preventive Services Task Force (USPSTF) ve AUA 55 yaşında başlanmasını (25,26) önermektedirler. PSA taramalarına aile hikayesi pozitif olanlarda, siyah ırka mensup olanlarda normal popülasyona göre daha erken yaşlarda başlanmaktadır. BRCA bir DNA onarım genidir. NCCN(National Comprehensive Cancer Network) guideline’da BRCA1 ve 2 taşıyıcılarında PSA taramalarına 45 yaşında başlamayı, yüksek risk gurubu Pca açısından yada metastatik Pca açısından aile hikayesi pozitifliği olanlarda rutin BRCA1/2 testi yapılmasını önerilmektedir(27). IMPACT çalışmasında BRCA1/2 taşıyıcılığı ile Pca insidensi araştırılmıştır; BRCA2 mutasyonu taşıyanlarda taşımayanlara göre Pca insidansının daha yüksek olduğu(s), BRCA2 taşıyanlarda taşımayanlara göre kanserin daha erken yaşta tespit edildiği(s) ve bunlarda daha yüksek oranda klinik önemli kanser tespit edildiği(s), BRCA1 taşıyan ve taşımayanlar arasında tümör karekteristikleri açısından anlamlı fark olmadığı(ns), bu sebeple BRCA2 mutasyonu taşıyanlarda sistematik olarak PSA taramasının yararlı olacağı bildirilmiştir(27). Gelişmiş ülkelerde Pca sebebiyle mortalite oranlarının azalmasında tedavideki gelişmelerin (cerrahi, hormonal, radyoterapi) ve PSA testinin yaygın kullanımının rolünün büyük olduğu kabul edilmektedir(28,29).
-Göteborg-1 çalışmasında yaş aralığı 50-64 olan 10.000 erkeğe ve 10.000 kişiden oluşan kontrol gurubuna 1995 de PSA taramasına başlanmış olup 70 yaşına kadar 2 yıl aralıklarla devam ettirilmiştir. Carlsson et al Göteborg randomize prostat kanseri tarama çalışmasının 24 yıllık sonuçlarını değerlendirerek “daha genç yaşta PSA taramalarına başlamanın prostat kanseri sebebiyle mortaliteyi daha yüksek oranda azaltacağı” hipotezini ileri sürmektedirler(30,31). Carlsson et al nın “Prostat kanseri için Göteborg tarama çalışmasının” 24 yıllık sonuçlarını analizlerinde; daha genç yaşta PSA taramasına başlamanın Pca sebebiyle mortaliteyi daha yüksek oranda azalttığı, taramaya 55 yaşında başlamada 60 yaşında başlamaya göre Pca sebebiyle mortalitenin yarı yarıya azaldığı, PSA taramasına 55 yaş yerine 50 yaşında başlamanın daha yararlı olacağı, 75 yaş üzerinde tüm guruplarda Pca insidensinin benzer oranda olduğu bildirilmiştir(12).
-ERSPC’nin 1993-2003 yılları arasında yaş aralığı 50-74 olan 8 Avrupa ülkesinde randomize tarzda yaptığı PSA taraması çalışmasında; 182000 kişinin PSA taraması versus (vs) kontrol gurubuna randomize edildiği, 16 yıllık takipte PSA taraması yapılan gurupta prostat kanseri sebebiyle mortalitede(CSM’de) relatif olarak %20 azalma görüldüğü bildirilmiştir(5,11). Göteborg çalışmasında da 20000 kişinin 2 yılda bir PSA testi vs oportunistik PSA testine randomize edildiği, 18 yılda Pca için CSM’nin relatif olarak %42 azaldığı belirtilmiştir(7).
– Göteborg toplum bazlı randomize tarama çalışmasının 22 yıllık sonuçlarında Godtman et al; yaşta her 1 yıl artışta GS 3+4 Pca riskinin GS <7 Pca riskine göre %11 oranında arttığını, yaşın her 1 yıl artışında GS
4+3 Pca teşhisinin vs GS<7 Pca teşhisi riskine karşın %8.5 oranında arttığını, sonuçta yaşlanmanın artışıyla daha yüksek GS’lu Pca riskinin arttığını, Pca teşhisinde ortalama yaşın 65 olduğunu, teşhis edilen Pca’lerinin %81 nin GS<7 olduğunu, teşhis edilen prostat kanserlerinin %14 nün GS 3+4 olduğunu ve %5 nin de GS
4+3 olduğunu bildirmişlerdir(32).
Lokalize prostat kanserlilerden hiçbir tedavi almayanlarda prostat kanserinin tabii seyri
-Günümüzde risk gurubuna göre lokalize prostat kanserleri için aktif izlem (AS) (veya watchful waiting-WW), radikal prostatektomi (RP), radyoterapi (RT) veya brakiterapi (BT), fokal terapiler uygulanmaktadır. Bu tedavi seçenekleri uygulanırken temel amaç prostat kanseri sebebiyle mortaliteyi önleyebilmek yada azaltabilmektir. Ancak radikal tedavilerin gerekmediği hastalara radikal tedavileri uygulamak yarar yerine bazen zararlı sonuçlar yaratabilmektedir. Özellikle çok düşük yada düşük risk gurubu hastalara radikal tedavilerin uygulanması çoğu zaman tedavinin yarattığı morbiditeler sebebiyle zararlı olabilmektedir.
-İskandinav Prostat Kanseri Gurubu 4 ün(SPCG-4) çalışmalarında lokalize prostat kanserlilerde cerrahi (RP) ile izlem karşılaştırılmış olup 65 yaşın altındakilerde cerrahinin tüm sebeplerden mortalitede %12.7 azalma sağladığı bildirilmiştir(33-35). Düşük grade’li lokalize Pca’lerinde ise cerrahinin prostat kanserine spesifik mortalite (PCSM) açısından çok yararlı olmadığı ileri sürülmektedir. PIVOT çalışmasında ise 12 yıllık takipte düşük grade hastalığı olanlarda hastalığa spesifik mortalite ve tüm sebeplerden mortalite riskinde cerrahinin bir azalma sağlamadığı belirtilmiştir(36). Gerek İskandinav çalışmasında gerekse PIVOT çalışmasında hastaların yarıdan çoğunun 65 yaş üzerinde olduğu bilinmektedir. Günümüzde düşük grade’li hastalar için aktif izlem (active surveillance, AS) sonuçları ile bu veriler genel olarak uyumlu görünmektedir.
-65 yaş ve üzerinde, hiçbir tedavi almayan (cerrahi, radyoterapi, fokal tedaviler veya hormon tedavisi uygulanmayan) hastalarda prostat kanserinin 15 yıllık sonuçlarının bildirildiği Yao et al nın çalışmalarında da; araştırmanın 1992-2009 dönemindeki 31137 hastayı kapsadığı, evrenin T1-T2 olduğu, kanser teşhisinden sonra 6 ay içinde ölen yada bir başka tip kanser teşhis edilenlerin, herhangi bir tip tedavi alanların, grade’i bilinmeyenlerin, evresi T1a-T1b olanların değerlendirme dışı bırakıldığı, ilk teşhiste ortalama yaşın 75 olduğu, yaşayan hastalarda ortalama takibin 6.4 yıl olduğu, hastaların çoğunda (%87 sinde) GS’nun 5-7 olduğu, %40 ının T1c olduğu, sağ olan hasta sayısının 10 yılda 5257 ve 15 yılda 1138 olduğu, GS 5-7 gurubunda 15 yıllık kansere özgü mortalite oranının 65-74 yaş gurubunda %5.7 ve 75 yaş yada daha üstündekilerde %10 olduğu, T1c gurubunda olup GS 8-10 olanlarda 15 yıllık kansere özgü mortalite oranının 65 yaş altındakilerde vs 65-74 yaştakiler sırayla %22 ve %27 olduğu, sonuç olarak ilk teşhiste GS 5-7 olup T1c evresindekilerde 15 yılda kansere özgü mortalite oranının %10 dan az olduğu ve 15 yılda ortalama yarısına kanser tedavisi(RP, RT veya ADT) gerekmediği, GS 8-10 hastaların konservatif izleminin kansere özgü mortaliteyi arttırdığı bildirilmiştir(37).
– SEER verileri baz alınarak 1992-2005 arasında RP yapılan veya izlem protokolü uygulanan lokalize Pca’li 44694 hastada risk guruplarına göre survival etkilenmesinin araştırıldığı Abdollah et al nın çalışmasında 10 yıllık kanser spesifik mortalite oranları yüksek risk gurubunda olup RP yapılanlarda %5.2 vs yüksek risk gurubunda olup izlem yapılanlarda %12.8 bulunmuştur, düşük-orta risk gurubunda RP yapılanlarda kanser spesifik mortalite %1.4 vs düşük-orta risk gurubunda olup izlem yapılanlarda kanser spesifik mortalite %3.8 bulunmuştur(38). Yaşa göre değerlendirildiğinde kansere özgü mortalite oranları 65-69 yaş gurubunda RP yapılanlarda %2 vs izlemdekilerde %4.6, 70-74 yaş gurubunda aynı değerlendirme sırayla %2.6 vs %5.6, 75-80 yaş gurubunda aynı değerlendirme sırayla %2.7 vs %8.1(her biri için p<0.001) bulunmuş olup çok yönlü analizlerde Pca’ne spesifik mortalite için tüm kategorilerde RP nin bağımsız prediktör olduğu, RP den en çok yüksek risk gurubu hastaların yararlandığı, en az yararlanmanın düşük-orta risk gurubunda olduğu belirtilmiştir(38).
Metastatik prostat kanserlerinin seyri
-Metastatik prostat kanserleri ilk teşhis edildiğinde metastatik olanlar ve lokal tedaviden sonra (RP, RT, brakiterapiden sonra) metastaz gelişenler olarak incelemek gerekir.
1-İlk teşhiste metastatik olanlar
-İlk teşhiste metastatik prostat kanserine ileri yaşlarda daha genç popülasyona göre daha yüksek oranda rastlanmaktadır. Amerikada 1998-2007 döneminde 464918 Pca tespit edildiği, bu hastalar yaş guruplarına göre ayrıldığında ilk teşhiste M1 Pca oranının 75 yaşından küçük kişilerde %3, 75-79 yaşlarda %5, 80-84 yaşlarda %8, 85-89 yaşlarda %13, 90 yaş ve yukarısında %17 olarak bulunduğu, 75 yaşından küçük hastalar için 5 yıllık kümülativ ölüm insidensinin %3-4 olduğu ve bu oranın 75-79 yaş için %7, 80-84 yaş için %13, 85-90 yaş için %20, 90 yaş ve üzerinde olanlarda %30 olduğu bildirilmiştir(39). 75 yaş ve üzerindekilerde Pca %26 olmasına rağmen bunların %48 i M1vakalar olduğu belirtilmiştir. Bu çalışmadan “yaşlandıkça metastatik Pca oranının arttığı ve Pca’den ölüm riskinin arttığı” sonucu görülmektedir.
-Önceki yıllara ait çalışmalardan Tangen et al nın çalışmasında “kemik metastazlı Pca’lilerin ortalama %50 sinin 2-3 yılda, %75 nin 5 yılda Pca sebebiyle öldüğü, %10 nun 10 yıldan fazla yaşayabildiği” belirtilmiştir(40). Bu çalışmada 10 yıl yada daha fazla yaşamada prediktif faktörlerin “hastalığın minimal olması, iyi performans durumu, kemik ağrısı olmaması, GS nun ≤7 olması ve düşük PSA değeri” olarak belirtilmiştir. Tedaviye başlamadan önceki PSA seviyesinin survival’ı öngörmede etkili olmadığını belirtenler yanında(41) tedaviye başladıktan sonra ulaşılan nadir PSA seviyesinin survival için prediktör olduğunu belirtenler(42) de vardır. SWOG S8494, S8894 ve S9346 çalışmalarında metastatik Pca’lerinde ortalama tüm sağ kalımın 30-49 ay arasında değiştiği bildirilmiştir(43). ABD’de ilk teşhis edildiğinde Pca’lerinin %4 ünün metastatik olduğu, Danimarka’da yapılan araştırmada da bu oranın %3 olduğu, 1 ve 5 yıllık survival’ın %47 ve %3 olduğu belirtilmiştir(44). Diğer çalışmalarda da metastatik Pca’lilerde ortalama survival’ın 24-48 ay olduğu belirtilmektedir(45). Metastatik Pca’lilerde survival ile ilgili bu veriler bu gurup hastalarda sadece ADT uygulandığı dönemlerin verileridir, son yıllarda ADT ile birlikte yeni jenerasyon androjen reseptör inhibitörlerinin (abirateron veya enzalutamid yada benzerleri) yada ADT ile birlikte kemoterapötiklerin (docetaxel) kullanılmasıyla tüm sağ kalımda daha iyi sonuçlar alınmaktadır.
– EAU-EANM-ESTRO-ESUR-SIOG Prostat Kanseri-2020 guideline’da; yeni teşhis edilmiş metastatik Pca’de ADT monoterapi ile tedavide ortalama survival’ın 42 ay olduğu, tedaviye cevabı ve survival’ı etkileyebilecek birçok prognostik kriterin var olduğu (kemik metastazlarının sayı ve yeri, visseral metastaz olup olmaması, ISUP grade’i, hastanın performans durumu, başlangıç PSA değeri ve alkalen fosfataz değeri gibi), bunlar içinde en kritik önemde olanın hastalığın volümü olduğu, standart ADT’ne docetaxel ilave edilmesinin 4 yılda survival’da %9 mutlak iyileşme sağladığı, kontrendikasyon olmadıkça metastatik Pca’lilerde standart ADT’ne ilave tedavilerin yarar sağladığı belirtilmiştir(46).
2-Radikal (definitif) lokal tedavilerden sonra metastaz gelişenler
-Loeb et al “RP yapılmış ve sonradan metastaz gelişmiş, hormon naive 193 hastanın analizinde metastazın post-op ortalama 6 yıl sonra geliştiğini, metastaz geliştiğinde ortalama PSA’nın 31.9 ng/ml olduğunu, metastaz gelişen 50 hastada(%25.9) PSA<10 ng/ml olduğunu, metastazın düşük PSA seviyelerinde bile gelişebileceğini, bu sebeple RP sonrası biyokimyasal nüks gelişenlerde dikkatli takip gerektiğini bildirmişlerdir(47). Metastaz gelişen bu 193 hastada metastaz geliştiğinde PSA aralığı 0.2-2901.9 ng/ml arasında değişmekte olup metastaz gelişen 6 hastada PSA’nın 1 ng/ml den az olduğu dikkat çekmektedir. Pound et al RP yapılmış biyokimyasal nükslü 315 hasta gurubundan 103 hastada (%34) post-op biyokimyasal nüksden metastaza kadar geçen sürenin ortalama 8 yıl olduğunu bildirmişlerdir(48).
-Makarov et al 1987-2005 döneminde RP yapılmış 3096 hastanın 422 sinde sonradan PSA nüksü geliştiğini, bunlardan da 123 ünde uzak metastaz geliştiğini, metastaz görüldükten sonra ADT uygulandığını, toplam 41 hastanın Pca sebebiyle öldüğünü, ortalama takibin 120 ay olduğunu, RP sonrası PSA nüksü için geçen ortalama sürenin 24 ay olduğunu, PSA nüksünden sonra metastaza kadar geçen ortalama sürenin 36 ay olduğunu, metastazdan ölüme kadar geçen ortalama sürenin 84 ay olduğunu, RP den ölüme kadar geçen ortalama sürenin de ortalama 168 ay olduğunu, çok yönlü analizlerde kansere özgü mortalite için “metastaza kadar geçen sürenin, metastaz bulunduğunda ağrının var olmasının ve PSADT’ın 3 aydan daha kısa olmasının” bağımsız prediktörler olduğunu(sırayla p=0.003 ve p=0.017) bildirilmişlerdir(49). Bu verilerden RP yapılmış hastalarda sonradan PSA nüksü gelişse bile metastaza kadar hatta ölüme kadar geçen sürenin hastaların çoğunda azımsanamayacak derecede uzun olduğu, ayrıca RP sonrası BCR durumunda metastaz gelişmeden ADT uygulanmadığı görülmektedir.
-Shikanov et al nın SEER verileri baz alınarak 1988-2003 arasında dönemde 127236 RP vakasında RP’den sonra prostat kanserine özgü mortalite (CSM) oranlarını araştırdıkları çalışmalarında; ortalama takibin 7.2 yıl olduğu, RP’den sonra 5 , 10 ve 15 yılda kansere özgü mortalite oranlarının tüm hasta gurubunda sırayla %0.4, %0.7 ve %1 olduğu, tüm gurup için 5, 10 ve 15 yıllık prostat kanserine özgü survival oranlarının sırayla %98, %95 ve %90 olduğu, çok değişkenli analizlerde de kansere özgü survival’ı olumsuz etkileyen ve anlamlı derecede bağımsız ilişki gösteren faktörlerin “yüksek evre, yüksek grade, ileri yaş ve siyah ırk” olduğu bildirilmiştir(50). Eggener et al’nın 2011 deki çalışmasında 11521 RP vakasının analizinde 15 yıllık Pca’ine özgü mortalitenin %7 olduğu, GS’una göre bu mortalite oranının GS≤6, GS 3+4, GS 4+3, GS 8-10 olanlarda sırayla %0.2-1.2, %4.2-6.5, %6.6-11, %26-37 aralığında değiştiği, 15 yıllık Pca’ine özgü mortalite riskinin organa sınırlı hastalıkta %0.8-1.5, ekstraprostatik yayılımda %2.9-10, SVI varlığında %15-27 ve lenf nodu tutulumunda ise %22-30 olduğu, organa sınırlı hastalığı olan GS≤6 9557 hastadan sadece 3 ünün Pca’den öldüğü bildirilmiştir(51).
-Johns Hopkins’de 1982-2011 arasında tek cerrah tarafından (Walsh PC) gerçekleştirilmiş 4478 RP nin ortalama 10 yıllık takipli (range 1-29 yıl) analizinde “25 yıllık progresyonsuzluk, metastazsızlık ve kansere özgü sağ kalım oranlarının” sırayla %68, %84 ve %86 olduğu, PSA öncesi dönem ile PSA dönemi arasında sonuçlar yönünden anlamlı farklılık bulunduğu belirtilmiştir. D’Amico risk guruplarına göre değerlendirildiğinde progresyonsuz, metastazsız survival ve kansere özgü sağ kalımlarda risk gurupları arasında anlamlı derecede farklılık olduğu, çok yönlü analizlerde patolojik evre ve grade’in metastatik progresyon ve kansere özgü ölüm için anlamlı derecede birliktelik gösterdiği bildirilmiştir(52).
-Radikal tedavilerden sonra metastaz riskini, Pca sebebiyle ölüm riskini etkileyen önemli faktörlerden biri PSADT’dır. Radikal tedavilerden sonra metastaz gelişenlerden PSADT 15 aydan uzun olanlarda Pca’ne özgü mortalitenin (PCSM) 10 yıldan uzun sürede düşük oranda olduğu, PSADT 3 aydan kısa olanlarda ise PSA nüksünden itibaren ortalama genel sağ kalımın 6 yıl olduğu belirtilmiştir(53,54). Pca için RT görmüş, aynı zamanda ADT almış yada almamış hastalarda PSADT<8 ay olanlarda metastatik hastalıktan ölüm riskinin anlamlı derecede yüksek olduğu birçok araştırmacı tarafından bildirilmiştir(55,56).
Lokalize prostat kanseri için lokal tedaviden (radikal prostatektomi, radyoterapi) survival’a katkı açısından yararlanabilecek hastaların özellikleri
-Burada yarardan kasıt “survival’a katkı, ömrü uzatmaya katkı, Pca sebebiyle ölümü yada ölüm riskini azaltabilmek”tir. Yaş göz önüne alındığında genel kabul gören kriterlere göre Pca için lokal tedavilerden en çok 70 yaş ve altındakiler yarar görmektedir. Pca için lokal tedavilerden en yüksek oranda 70 yaş ve altındakilerin yarar gördüğü kabul edilmektedir. Ancak son yıllarda bu kriterde bazı esaneklikler gelişmiştir; “yaşı 70 yada daha yüksek olduğu halde yüksek grade’li ve agressiv özellikte lokalize Pca tespit edilenlerde de lokal tedavilerin uygulanması bu kişilerin Pca sebebiyle ölmesi riskini azaltacaktır” görüşü kabul görmektedir. Yaş ilerledikçe beklenen ömür kısalmasına rağmen agressiv Pca insidansı artmaktadır, agressiv (yüksek riskli) lokalize Pca olan ve yaşı 70 yada daha yüksek kişilerde RP yapılması bu kişilerin Pca sebebiyle ölüm riskini azaltacaktır.
-Lokalize Pca’liler arasında lokal tedavilerden survival açısından en çok yarar görenler yüksek risk gurubu kanserlilerdir. Yüksek risk gurubundaki hastalara çoğu zaman multimodal tedavi uygulanmaktadır. Johns Hopkins’den yapılan çalışmada 1992-2008 arasında yapılan RP’lerden 175 hastanın yüksek risk gurubunda olduğu, bunlardan sadece 63 hastada (%36) RP spesmenlerinde organa sınırlı hastalık görüldüğü, 10 yılda rekürrenssiz survival’ın %68, metastazsız survival’ın %84, Pca’ine özgü survival’ın %92 olduğu, 10 yılda hormonal terapi gerekmeme durumunun %71 olduğu,
-biyokimyasal nüks, metastaz ve Pca sebebiyle ölüm için en güçlü bağımsız prediktörün biyopsi GS 8-10 olduğu, sonuçta yüksek risk gurubundaki dikkatli seçilmiş hastalarda RP ile uzun süreli progresyonsuz sağ kalım sağlanabildiği bildirilmiştir(57).
-Yaşlı popülasyonda lokal tedavilerin agressiv özellikli kanserlilerde yararı olmakla birlikte bazı araştırmalarda lokal tedavilerin izleme üstünlük göstermediği belirtilmiştir. Cancer Group Trial Number 4 çalışmasında izlem (watchful waiting, WW) vs radikal prostatektomi (RP) çalışmasında RP nin 65 yaşından küçüklerde prostat kanserine özgü mortalitede anlamlı derecede iyileşme sağladığını fakat daha yaşlılarda WW ile RP arasında prostat kanserine özgü mortalite açısından anlamlı farklılık olmadığını bildirmişlerdir(58).
-Bill-Axelson et al “lokalize prostat kanserinde radikal prostatektomi yada izlem (watchful waiting)” prospektif-randomize çalışmalarının daha önceki sonuçlarını ve 29 yıllık sonuçlarını bildirmişlerdir(33,59). İzlem vs RP gurupları arasındaki ölüm oranı yönünden mutlak farklılığın %12 olduğu, 10. yılda tüm sağ kalım yönünden RP nin mutlak yararı %5 iken 23. yılda bu oranın %12 ye ulaştığı (RP nin yararının 10 yıldan sonra daha belirgin olarak görülmeye başlandığı), GS 4+5 yada daha yüksek skorlularda mortalite riskinin 10 kat artmış olduğu, ekstrakapsüler yayılımın (EPE) mortalite riskini arttırdığı fakat pozitif cerrahi marjinin (PSM) bu risk artışına etkili olmadığı bildirilmiştir(59). Bu çalışmaya Taneja SS tarafından yapılan editoryal yorumda; çalışmaya hasta alımının 1988-1989 da başlandığını, hastaların o dönemde klinik muayene ve sextant biyopsi ile değerlendirildiğini, PSA kullanılmadığı için erken evre Pca’lerinin (T1c kanserler) bulunmadığını, bu sebeple izlemin tüm guruba genellenemeyeceğini belirtmiştir(60).
-Yaşlı popülasyonda radikal tedavilerde göz önüne alınması gereken bazı hususlar vardır,bu konuda SIOG(Task Force of the International Society of Geriatric Oncology, SIOG) önerilerde bulunmaktadır. 2014 den beri bildirilen SIOG kriterleri ile EAU/ESTRO kriterlerinin uyumlu olduğu bilinmektedir. Bu önerilerde “ yüksek riskli Pca’li, sağlıklı yaşlı hastalara genellikle undertreated (eksik yada uygunsuz, effektif olmayan tedaviler) yapıldığı, bunun yanında birçok düşük riskli, komorbiditeleri olan yaşlı hastalara da overtreatment yapıldığı, yaşlı ve yüksek grade’li Pca olan birçok hastanın RP’den yararlanabileceği” belirtilmiştir(61).
– Yaş-agressiv prostat kanseri ilişkisi yaş artışına paralel artmaktadır. Agressiv özellikli prostat kanserlerine ve metastatik prostat kanserlerine elli yaşından önce de rastlanabilmektedir. Thorstenson et al nın 50 yaşından önce Pca teşhis edilenlerde kansere özgü mortaliteyi araştırdıkları çalışmalarında “tüm yaş guruplarında yaş arttıkça Pca insidansı artmakla birlikte tüm yaş guruplarında metastatik Pca insidansının benzer olduğu, genç yaş gurubunda düşük risk gurubu Pca’nin daha sık olduğu ve yaşlı hasta gurubunda da yüksek risk gurubu non-metastatik hastalığın daha sık olduğu, ilk teşhiste nonmetastatik Pca teşhis edilenlerde kansere özgü mortalinin yaşa paralel arttığı, 50-55 yaşından önce metastatik Pca kanseri tespit edilenlerde “genç yaş-prostat kanserine özgü mortalite” ilişkisinin oldukça yüksek olduğu, bu sonucun genç yaşlarda tespit edilen Pca’lerinin yaşlılarda tespit edilenlerden biyolojik olarak farklı olduğunu düşündürdüğü, aksine nonmetastatik Pca’lilerde yaşın önemli bir faktör olmadığı” belirtilmiştir(62).Genel sonuçların aksine45-55 yaş grubunda tespit edilen Pca’lerinin daha yaşlılardakine göre diferansiasyon derecesinin daha kötü olduğunu, daha agressiv bir fenotip gösterdiğini bildiren çalışmalar bulunmaktadır(63-65). Bratt et al genç yaş gurubunda metastatik Pca tespit edilenlerde prognozun daha ileri yaşlarda metastatik Pca tespit edilenlere göre daha kötü olduğu bildirilmiştir(66). Birçok araştırmacının belirttiği gibi PSA testi kullanıma girmeden önce tespit edilen Pca’lerinin özelliği ile PSA kullanıma girdikten sonra tespit edilenlerin özellikleri arasında farklılıklar bulunmaktadır, çalışmalar değerlendirilirken bunu dikkate almak gerekir. Araştırmacılar genç yaşta Pca tespit edilenlerde germline mutasyonun ve hereditenin Pca’nin sebebi olabileceğini belirtmektedirler(62). Yüksek grade’li ve ileri evre prostat kanserlerinde olduğu gibi herediter göğüs ve over kanserlerinde sıklıkla BRCA2 mutasyonu bulunduğu belirtilmektedir. Bir başka araştırmada da DNA onarım genleri olan BRCA1, BRCA2, ATM ve CHEK2 genlerinde mutasyonuna familyal Pca vakalarının %7.3 ünde rastlandığı, BRCA2 mutasyonunun %29 oranında en sık rastlanan mutasyon olduğu belirtilmiştir(67). Birçok araştırmada aile hikayesinde anne tarafında meme kanseri hikayesi pozitif olanlarda Pca riskinin aile hikayesi negatif olanlara göre artmış olduğu belirtilmektedir.
Lokalize prostat kanseri için lokal tedaviden sonra gelişebilecek metastaz ve prostat kanseri sebebiyle ölümün prediktörleri
1–Gleason skoru(GS)
-Lokalize Pca’lilerde nüks, progresyon, metastaz ve Pca sebebiyle ölüm açılarından en başta gelen kriter spesmenin histopatolojisinin Gleason skorudur. Gleason skor 8-10 olan hastalar yüksek risk gurubuna giren hastalardır, GS 8-10 olması progresyon için anlamlı derecede bir risk faktörüdür. GS 8-10 olan hastaları tüm gurup olarak değerlendirme yanında bunlardan içinde Gleason grade 5 olanları ayrı değerlendirmenin GS 8-10 olduğu halde Gleson grade 5 olmayanları ayrı değerlendirmenin prognoz açısından daha doğru olacağı bazı araştırmacılarca belirtilmektedir. Bu araştırmacılar Gleason grade 5 komponentinin var olmasının gerek yüksek risk gurubunda gerekse orta risk gurubunda klinik progresyon riskini ve kötü sonuçlar riskini (metastaz gibi) anlamlı derecede arttırdığını belirtmektedirler(68-71).Stroup et al da “biyopside Gleason grade 5 tespit edilip radikal prostatektomi yapılanlar ile yüksek risk gurubunda olan Gleason 8-10 skorlu fakat grade 5 komponenti olmayan ve radikal prostatektomi yapılanların biyokimyasal nüks, klinik nüks, metastaz ve mortalite açısından karşılaştırılması “ amacıyla yaptıkları araştırmada Gleason grade 5 komponenti var olmasının progresyon, metastaz, kansere özgü ölüm, tüm sebeplerden ölüm için daha yüksek risk taşıdığını bildirmişlerdir(72). Tersiyer grade primer ve sekonder grade’lerden daha yüksek ise ise patoloji raporlarında bu durum belirtilir, daha düşükse belirtilmez. Tersiyer grade primer ve sekonder grade’den daha yüksekse anlamlı derecede kötü bir patolojik göstergedir. Tersiyer grade’in minimal bir parçada olmasının klinik önemi tam bilinmemektedir. Montironi et al 2005 ISUP kararlarında RP spesmenlerinde tersiyer grade 5 var olması halinde bunun tümörün %5 den azını yada %5 den fazlasını işgal edip etmediğinin belirtilmesinin önerildiğini belirtmiştir, 2014 ISUP kararlarında ise RP spesmeninde tersiyer grade 5 in sadece GS 3+4=7 veya GS 4+3=7 vakalarında belirtilmesinin önerildiği bildirilmiştir(73,74).
-Yüksek yada çok yüksek risk gurubu hastalarda radikal tedaviler sonrası klinik nüks ve/veya metastaz gelişmesi riski düşük-orta risk gurubuna göre daha yüksektir. Yüksek risk gurubu Pca’lerinin özellikleri “klinik evre ≥ T3, başlangıç PSA > 20 ng/ml yada GS 8-10” olarak belirtilmektedir. Bu gurup klinik lokalize hastalara genel durumu uygunsa radikal tedavi olarak RP ve/veya RT, brakiterapi uygulanır. Bu gurup hastalarda primer radikal tedavilere çoğu zaman ADT eklenir. Kishan et al “2000-2013 döneminde biyopsi GS 9-10 olan EBRT(veya EBRT + BT) veya RP uygulanmış 487 hastanın analizinde “RT ve RP nin benzer oranda kansere özgü survival sağladığını ve benzer oranda tüm sağ kalım sağladığını, özellikle doz ayarlamalı RT + ADT nin sadece RT’ye yada sadece RP ye göre daha düzelmiş sistemik kontrol sağladığı bildirmişlerdir(75). Kishan et al başka bir raporlarında GS 9-10 Pca’lerinde ComboRT (EBRT + brakiterapi) + ADT alanlarda RP uygulananlara göre uzak metastazsızlık durumunun ve prostat kanserine özgü mortalitenin(PCSM) daha iyi olduğunu bildirmişlerdir(76). Diğer çalışmalarda RP + adjuvan RT’nin(aRT) ComboRT’ye benzer yada daha iyi sonuçlar verdiği belirtilmektedir(77-79). Tilki et al da GS 9-10 kanserli olup RP + aRT + ADT vs ComboRT + ADT karşılaştırmasında PCSM ve tüm sağ kalım(OS) yönünden anlamlı fark olmadığını bildirmişlerdir(80). Muralidhar et al ve Ennis et al Gleason skoru 9-10 lokalize prostat kanserlerinde “ RP + ADT sonuçlarıyla ComboRT sonuçlarının OS ve PCSM yönünden benzer olduğunu” bildirilmişlerdir(81,82). Berg et al “yüksek riskli lokalize prostat kanserlilerde radikal prostatektomi versus EBRT + brakiterapinin (BT) karşılaştırmalı etkinliğini araştıran çalışmalarında EBRT + BT uygulananlarda RP uygulananlara göre daha yüksek tüm sebeplerden mortalite tespit edildiğini(s), sağlıklı genç yüksek riskli lokalize Pca’li erkeklerde RP nin anlamlı derecede daha yüksek tüm sağ kalım sağladığını” bildirilmişlerdir(83).
2-Evre ve klinik risk gurubu
–NCCN guideline’ına göre yüksek risk gurubu (HR) “klinik evre> T3a, yada GS 8-10, yada pre-op PSA> 20ng/ml “ olarak, çok yüksek risk gurubu(VHR) da “klinik evre ≥ T3b, yada Gleason grade 5 veya beş yada daha fazla core’da GS 8-10 “ olarak tanımlanmıştır.
PSA taramalarının tabii sonucu olarak günümüzde tespit edilen Pca’lerinin çoğu lokalize evrede olmasına rağmen hala %10 unun lokal-ileri evrede olduğu belirtilmektedir(84). Guideline’larda lokal-ileri evre hastalarda nüks riskinin yüksek olduğu belirtilmekte ve bu sebeple bunlara küratif tedaviden ziyade sistemik tedavilerin uygulanması önerilmektedir. Ancak bu gurup hastalara cerrahi tedavi (RP) ve kombine tedavilerle(RT, ADT) iyi sonuçlar alındığını bildiren çalışmalar bulunmaktadır. Literatürde RP uygulanan lokal-ileri evre hastalarda 5 yıllık kansere özgü mortalitesiz survival’ın %90 dan fazla olduğu belirtilmektedir(85).
-İsveç’den Stattin et al nın gerçekleştirdiği çok yüksek risk gurubu prostat kanserlerinde radikal lokal tedavinin mortaliteye etkisini araştıran ve 80 yaşın altındaki hastaların alındığı çalışmada;1998-2012 döneminde oldukça yüksek risk(very high risk) kriteri olarak “T4 ve/veya PSA 50-200 ng/ml, herhangi bir N kategorisi ve M0” değerlerinin kabul edildiği, belirtilen dönemde 80 yaşın altında 106204 Pca tespit edildiği, bunlardan 7500 ünün(%7) oldukça yüksek riskli(very high risk) olduğu ve 10316 sının (%10) da lokal-ileri evrede olduğu, 1998-1999 döneminde oldukça yüksek riskli 65 yaşın altındakilerden %21 i radikal tedavi alırken 2012 döneminde bu oranın %41 e çıktığı, oldukça yüksek riskli ve lokal-ileri evre hastalarda fulldoz RT +ADT nin en çok uygulanan radikal tedavi olduğu(dönemlerde sırayla %8 ve %19) olduğu, oldukça yüksek riskli hastalarda tüm yaş guruplarında daha önce etkisiz kabul edilen radikal tedavinin kansere özgü ve tüm sebeplerden mortaliteyi anlamlı derecede azalttığı bildirilmiştir(86).
3-Radikal prostatektomi spesmeninde kötü (adverse) patolojik bulguların var olması
-RP sonucu histopatolojide kötü (adverse) patolojik göstergeleri olan hastalarda sonradan metastaz gelişmesi riski yüksektir. Bu kötü patlojik göstergeler “seminal vezikül invazyonu (SVI), lenf nodu invazyonu (LNI), ekstarprostatik yayılım (EPE)” olarak sayılabilir. Kötü patolojik göstergeleri olan hastalar bir anlamda yüksek risk gurubu hastalardır. Histopatolojide pozitif cerrahi marjin de (PSM) kötü patolojik gösterge olarak sayılabilmektedir. PSM’nin cerrahi teknikten kaynaklanıp kaynaklanmamasına göre bu durum tartışmalıdır. Kötü patolojik göstergeleri olan hastalarda ilerde metastaz gelişmesi riskini minimale indirebilmek için adjuvant tedaviler yada erken salvage tedaviler uygulanması rasyonel yaklaşım olarak kabul edilmektedir. Bunlara adjuvant yada erken salvage tedavi uygulanmasının hangisinin doğru olacağı tartışmalıdır. Bu özellikteki hastalarda sadece RP yapılması ve devamında izleme alınması genellikle uzun sürede iyi onkolojik sonuçlar sağlayamamaktadır. Ancak gereksiz adjuvant tedavilerin hastalarda istenmeyen morbiditelere de yol açabileceği bilinmektedir. Bu sebeple adjuvant tedavi kararında hassas davranılmalıdır. Adjuvan RT (aRT) “nüks gelişmeden, cerrahiden sonra 1-6 ay içinde prostat yatağına ± SV bölgesine ve pelvik LN’ları bölgesine RT uygulamak” olarak tanımlanmaktadır(87). Erken salvage RT (sRT) ise RP’den sonra “biyokimyasal nüks geliştiğinde PSA ≤ 0.5 ng/ml iken prostat yatağına ± çevre dokulara uygulanan RT” olarak tanımlanmaktadır. Abugharib et al optimal tümör kontrolü için PSA’nın 0.5 ng/ml eşik değerini beklemenin gereksiz olduğunu yani uygulanacak sRT’nin PSA’nın bu sınırı geçmeden uygulanmasının yararlı olacağını belirtmektedirler(88). Spratt et al ise RP sonrası BCR’lü hastalarda sRT +ADT uygulamasıyla uzak metastazsız survival ve tüm sağ kalım yönlerinden en çok yararı “sRT öncesi yüksek PSA değeri olanların (PSA≥0.7 ng/ml), PSM’lilerin ve GS-8-10 olanların” gördüğünü belirtmektedirler (89). aRT’nin kötü patolojik göstergeleri olan hastalarda biyokimyasal nüks gelişmesini aRT yapılamayanlara göre anlamlı derecede azalttığı bilinmekle birlikte yukarda belirtilen özellikteki tüm hastalara aRT gerekip gerekmediği bilinmemektedir, ayrıca RT’nin erken ve geç komplikasyonlarını da dikkate almak gerekmektedir. Bu sebeple RP’de kötü patolojik göstergeleri bulunan hastalara aRT mi yoksa BCR görüldüğünde erken sRT mi uygulanması gerektiği tartışmalıdır. Abdollah et al RP’ye ilave olarak aRT uygulanan ve uygulanmayan 1000 hastada yaptıkları araştırmada LNI, SVI, GS 8-10 karekterlerinden en az 2 sini bulunduranlarda aRT nin 10 yılda kansere özgü sağ kalımda %10.3 iyileşme etkisi gösterdiğini bildirmişlerdir(90). LN pozitif 773 hastada yapılan araştırmada da aRT nin BCR’süz ve metastazsız survival’ı anlamlı derecede iyileştirdiği belirtilmiştir(91). aRT nin uygun olduğu hasta gurubunu seçmede yeni geliştirilen genomik sınıflama skorunun yararlı olduğu, bu skorlamanın 24 gen’e dayandığı, yüksek skorlu hastalarda aRT uygulananlarda 10 yılda metastaz riskinin %4 vs uygulanmayanlarda %35 olduğu belirtilmiştir(92). 1100 den fazla erken sRT uygulanan hastada yapılan bir araştırmada 10 yılda BCR’siz survival ve metastazsız survival’ın sırayla %35 ve %80 olduğu bildirilmiştir(93). 500 den fazla pT3N0 hastayı kapsayan aRT vs erken sRT ile ilgili bir araştırmada sRT nin PSA≤0.5 ng/ml iken uygulandığı, 8 yıllık takipte metastazsız survival ve tüm sağ kalım yönünden iki gurup arasında anlamlı fark görülmediği bildirilmiştir(94). Erken sRT nin aRT’ye göre üriner fonksiyonların kötü etkilenmesi açısından daha az toksik etki gösterdiği belirtilmektedir(95).
-Onkolojik sonuçlar açısından genelde adjuvan ve erken salvage RT uygulamalarının benzer sonuçlar verdiği görülmektedir.
4-Biyokimyasal nüks
-Yüksek risk gurubunda olan lokalize Pca’lilerde lokal tedavilerden sonra düşük-orta risk gurubunda olanlara göre biyokimyasal nüks (BCR) gelişmesi riski de daha yüksektir. BCR her zaman klinik nükse dönüşmeyebilmektedir yani bazıları klinik nükse evrilen, daha ötesi metastaza kadar varabilen bir ilerleme gösterirken bir kısmında ise bu süreç gelişmemektedir. Lokalize Pca için radikal tedaviler gören hastaların ortalama %35 inde biyokimyasal nüks gelişmektedir. BCR sebebinin lokal nüks olduğu tespit edildiğinde hastaya primer tedavi olarak radyoterapi (RT) uygulanmışsa salvage RP, salvage fokal tedaviler, salvage irradiation (stereotactic body RT gibi) uygulanabilmektedir. BCR gelişen hastalardan primer tedavi olarak RP uygulanmış olanlara da sadece ADT, salvage RT ADT, salvage lenf nodu diseksiyonu gibi alternatifler uygulanabilmektedir.
-Knipper et al lokalize Pca için RP uygulanmış ve sonradan BCR gelişmiş hastalarda PSMA PET/CT’de retrovezikal sahada/seminal vezikül yatağında lokal nüks geliştiği tespit edilenlerde intraoperatif gamma probe kullanarak nükse sebep olan lezyonların salvage cerrahi ile çıkartılması (radioligand surgery) çalışmalarında; salvage cerrahi sonrası ortalama 24.4 aylık takipte %55 hastada BCR geliştiği ve 12 hastanın ilave tedaviler aldığı (ADT, RT, salvage LND, kombine kemo-hormonal tedavi), 1 yıllık takipte biyokimyasal nükssüz survival oranının %62.2 olduğu, tedavi gerektirmeyen survival’ın ortalama 46.3 ay olduğu, bildirilmiştir(96). 24 aylık takipte BCR oranının yüksekliği dikkat çekicidir. RP sonrası lokal nüks gelişen hastalarda lokal nüks yeri her zaman SV yatağı olmayabilir, örneğin anastomoz hattında gelişen bir lokal nükse salvage cerrahi uygulamak oldukça güç olsa gerekir, böyle bir durumda hastaya üriner diversiyon da yapmak gerekebilecektir. Per-op gamma-probe ile lokal nükse sebep olan lezyonun tespiti her zaman uygulanması kolay olan bir teknik değildir ve teknik zorluklar olabilmektedir.
– de Barros et al nın “radikal prostatektomiden sonra lokal nüks gelişen hastalarda lokal nüks için radio-ligand salvage surgery” sonuçlarında da komplet biyokimyasal cevap (cBR) oranı %29 bulunurken daha önce RT görenlerde cBR sağlanamadığı bildirilmiştir(97). Gerek Knipper et al nın gerekse de Barros et al nın sonuçlarına göre “radikal tedavi sonrası lokal yada bölgesel LN’larında nüks gelişen hastalara salvage cerrahi sonuçlarında umulan yararın alınamadığı görülmektedir. Salvage LND sonrası persistent PSA yüksekliği birçok hastada devam etmektedir, bu durum “metastatik lezyonların incomplete rezeksiyonu” olarak yorumlanmaktadır (98-101).
-Radikal prostatektomiden sonra sadece lenf nodlarında nüks görülen hastalarda salvage lenf nodu diseksiyonunun uzun süreli sonuçlarının araştırıldığı Bravi et al nın çalışmasında; 10 ve 12 yılda biyokimyasal nükssüzlük oranının %11 ve %9 olduğu, sLND’dan sonra BCR gelişmesi için geçen ortalama sürenin 22 ay olduğu, 110 hastada (%58) klinik nüks geliştiği (iskelet sisteminde, retroperitonda, pelvik bölgede, prostatik fossa’da, visseral organlarda), sLND’dan sonra klinik nüks gelişmesi için geçen ortalama sürenin 63 ay olduğu, 10 ve 12 yılda klinik nükssüzlük (metastaz free) oranlarının %31 ve %29 olduğu, klinik nüks gelişenlerin çoğunun sLND’dan sonra 5 yıl içinde geliştiği, sonuç olarak PET/CT de LN nüksü tespit edilip sLND yapılanların uzun sürede 1/3 nün Pca sebebiyle öldüğü, tek başına sLND’nu ile uzun sürede çok az hastada kalıcı cevap alınabildiği, çoğuna ilave tedaviler gerektiği bildirilmiştir(100).
-Yüksek risk gurubu yada lokal ileri evre prostat kanserlilerde biyokimyasal nüksden sonra, nüks ve metastaz riskini azaltmak amacıyla RP’den sonra ADT’ne ilave olarak yada ADT uygulanmadan doğrudan kemoterapi (docetaxel) uygulamaları da yapılmaktadır. Ancak bu uygulamadan umulan yarar görülmemiştir. Advanced Prostate Cancer Concensus Conference (APCCC) 2017 sonuçlarında hormonal tedavi almamış lokal-ileri evrede olup BCR gelişmiş hastalarda docetaxel tedavisinin yararı olmadığı bildirilmiştir.
5-Lenf nodu pozitifliği:
–Lenf nodu pozitifliği de yüksek risk bulgularından ve RP’de kötü(adverse) patolojik bulgulardan biridir. Diğer bir ifadeyle lenf nodu pozitifliğine düşük risk gurubunda olan hastalarda, düşük GS’lu hastalarda rastlamak zordur. Pelvik lenf nodlarında klinik olarak pre-op pozitif bulguya rastlanması ile RP sonucunda pozitifliğe rastlanması farklı durumlardır. Pre-op değerlendirmede pelvik lenf nodlarında pozitif bulguya rastlanması durumunda hastada uzak metastaz yoksa bu hasta “lokal-ileri evre” olarak değerlendirilir, bu durumda RP yapıp yapmama kararı tartışmalıdır. RP ve birlikte extended PLND yapıldığında LN pozitifliği olması durumunda LN sonucu negatif bulunanlara göre takiplerde BCR, klinik nüks, metastaz gelişmesi riskleri daha yüksektir. Pelvik lenf nodlarından daha öteye yani retroperitoneal bölge lenf nodlarına yada başka bölge lenf nodlarına yayılım varsa hastada beraberinde kemik yada visseral metastaz olmasa bile “metastatik prostat kanseri” olarak değerlendirilir. Düşük risk gurubu için aktif izlemin yaygınlaşması sonucunda RP için seçilen hastaların ortalama %50 nin yüksek risk gurubu hastalardan oluştuğu, RP materyellerinin histopatolojisinde önceki dönemlere göre pelvik lenf nodlarında metastazda (PLNM) artış olduğu, bu artışın RP için hasta seçiminde bias’dan kaynaklanabileceği belirtilmektedir(102).
-Radikal prostaektomi sonrası LN metastazı gelişenlerde prognoz: RP sonrası post-op dönemde LN metastazı gelişenlerde yada tespit edilenlerde prognozun kemik yada visseral organ metastazı gelişenlere göre daha iyi olduğu bilinmektedir. Bu sebeple nüks tespit edilen LN’larının tedavisinin hastalığın lokal kontrolüne maksimal fayda sağlayabileceği düşünülmektedir. RP sonrası LN metastazı gelişen ve visseral metastazı olmayanlarda uygulanabilecek tedaviler “ADT, RT, ADT + RT, salvage LN diseksiyonu” olarak sayılabilir. RP sonrasında LN metastazları diğer gereçlere göre sensitivite ve spesivitesi daha yüksek olan PSMA PET/CT ile araştırılır. RP sonrası LN metastazı gelişenlere salvage LND robotik yada açık cerrahi olarak yapılabilir. Salvage LND’nun vasküler ve üreteral yaralanmalar, lenfosel, lenfödem gibi bazı morbiditeleri vardır. Ancak salvage LND yapılmasına rağmen birçok hastada post-op BCR gelişebilmektedir, salvage LND’nun pre-op PET CT’deki sadece pozitif LN’larına değil, o bölgedeki tüm LN’larına yapılması önerilmektedir(103).
-Klinik olarak lenf nodu metastazı insidensi ve prognoz: Bernstein et al nın SEER verileri baz alarak günümüzde prostat kanserinde lenf nodu metastazının insidensini ve sonuçlarını araştırdıkları çalışmalarında; 2004-2014 dönemini kapsayan 443000 hastanın analiz edildiği, belirtilen dönemde metastatik olmayan Pca’nin yıllık insidensinin anlamlı derecede azalma gösterdiği, bu azalmanın hem 50-74 yaş gurubunda hem de 75 yaş ve üzerindekilerde görüldüğü, belirtilen dönemde metastatik olmayan Pca’de anlamlı azalmaya rağmen 50 yaş ve üzerindekilerde PLNM’da anlamlı derecede artış görüldüğü(s), PLNM’daki bu artışın hem RP yapılanlarda hem de RP yapılmayanlarda anlamlı derecede olduğu,
-analize alınan 443000 hastadan 417893 nün(%94.3) nonmetastatik, 6416 sının(%1.4) PLNM’lı ve 18691 nin de(%4.2) uzak metastazlı olduğu, bu 3 gurubun ortalama yaşlarının sırayla 66.0, 64.1 ve 70.6 olduğu, 50 yaş ve üzerindeki PLNM’lılarda prostat kanserine özgü mortalitenin(PCSM’nin) nonmetastatik olanlara göre anlamlı derecede daha yüksek olduğu, 75 yaş ve üzerindekilerde uzak metastazlılarda sadece PLNM’larında metastaz olanlara göre PCSM’nin anlamlı derecede daha kötü olduğu,
-son dekadda PLNM’daki bu artışın özellikle 75 yaş ve üzerindekilerde görüldüğü ve Pca taramalarında azalma ile birlikte seyir gösterdiği, bir diğer dikkat çeken hususun da özellikle minimal invaziv cerrahilerde artışla birlikte(robotik girişimler) RP’lerde PLND gerçekleştirmede azalma görülmesi olduğu, ayrıca düşük risk gurubu Pca’lilerde PLND gerekmeyebileceği önerilerinden de kaynaklanabileceği, başka bir sebebin de yüksek riskli hastalarda PET/CT ile görüntülerin PLNM oranını düşük tahmin etmiş olabileceği bildirilmiştir(102).
–Lenf nodu metastazı olanlarda tedavi sonuçları: Klinik olarak LN(+) olup ADT ile birlikte yada ADT uygulanmaksızın RP veya RT uygulanan 4 hastadan en az birinde 5 yıllık takipte klinik nüks geliştiği belirtilmiştir(104,105). Gandaglia et al klinik olarak lenf nodu pozitifliği olan hastalardan RP’den yararlanabileceklerin özelliklerini “pre-op konvansiyonal görüntüleme teknikleriyle şüpheli LN tespit edilen hastalardan biyopsi grade gurup 1-3 olan hastalar, şüpheli LN sadece pelvik bölgede olan hastalar” olarak belirtmişlerdir, tersine biyopsi grade gurup 4-5 ve retroperitonda şüpheli LN olanların onkolojik sonuçlarının kötü olduğunu yada RP’den yararlanma şanslarının düşük olduğunu bildirilmişlerdir(106). Gandaglia et al nın çalışmasına yapılacak en önemli eleştirilerin başında kendilerinin de limitasyon olarak belirttikleri gibi şüpheli LN’larının konvansiyonal görüntülemelerle belirlenmiş olması, PET/CT yönteminin kullanılmamış(yada değerlendirmelere alınmamış) olmasıdır.
-RP sonucu LN(+) bulunan hastalara uygulanması gereken strateji yada tedaviler hakkında tam bir görüş birliği bulunmamaktadır. Bunlara post-op dönemde cerrahi olarak salvage LND, hemen ADT’ne başlanması, BCR gelişirse ADT’ne başlanması, ADT ile birlikte RT uygulanması gibi farklı uygulamalar olmaktdır. NCCN guideline’ında bunlara metastaz yeri göz önüne alınmaksızın ilk tedavi seçeneği olarak ADT önerilmektedir(107). Zareba et al nın RP’de LN(+) bulunanlara uygulanan tedaviler ve sonuçlarıyla ilgili olarak National Cancer Data Base verilerine göre yaptıkları araştırmada; RP’de LN(+) bulunan 3680 hastanın analiz edildiği, takipte 641 hastanın öldüğü, RP den sonra yaşayanlarda ortalama takibin 5.9 yıl olduğu, RP den sonra 5 ve 10 yılda sağ kalım oranının %89 ve %66 olduğu, tüm sağ kalım oranının düşük olmasının (yada kötü olmasının) bağımsız prediktörlerinin “patolojik grade 4-5, patolojik evre T3b-T4, PSM” olduğu, çok değişkenli analizlerde RT+ADT kombinasyonunun Pca sebebiyle mortaliteyi izleme ve tek başına ADT’ne göre anlamlı derecede azalttığı(s), tek başına ADT yada tek başına RT nin izleme göre daha iyi tüm sağ kalım sağlamadığı bildirilmiştir(108).
-RP’de LN(+) bulunan hastalarda “kansere özgü mortalite ve tüm sebeplerden mortalitenin” ADT + RT uygulananlarda tek başına ADT uygulananlara göre anlamlı derecede daha düşük olduğu bildirilmiştir(104,109). Bir diğer bir çalışmada da pN1 hastalarda post-op undetectable PSA seviyesinin survival açısından bağımsız prediktör olduğu, diğer bir ifadeyle pN1 hastalarda post-op undetectable PSA seviyesi elde edilenlerde survival sonuçlarının daha iyi olduğu belirtilmiştir(110).
– Touijer et al nın “RP’den sonra LN(+) olan hastalarda survival sonuçları” nı araştırdıkları çalışmalarında da; EBRT + ADT alanlarda tüm sebeplerden ve Pca’den ölüm riskinin sadece ADT alanlara ve izlem gurubuna göre daha düşük olduğu(s), survival açısından ADT uygulananlarla izlem gurubu arasında anlamlı fark olmadığı(ns), sadece ADT alanlarda izlem gurubuna göre Pca’den ölüm oranının daha düşük olduğu(s), ömür boyu sadece ADT alanlarda diğer sebeplerden ölüm riskinin izlem gurubuna göre artmış olduğu(s) bildirilmiştir(111).
-RP yapılmış ve LN(+) bulunan hastalardan adjuvant RT’den yarar görebileceklerin araştırılmasında da; adjuvan RT’den en çok yarar görenlerin “bir yada iki pozitif LN’u olup patolojik GS 7-10 ve pT3b/T4” olanlar yada “pozitif cerrahi marjinliler ve üç yada dört pozitif LN’u olanlar” olduğu, adjuvant RT’den yarar görmeyenlerin yada daha az yarar görenlerin ise “bir yada iki pozitif LN’u olup patolojik GS 2-6 olanlar ve bir yada iki pozitif LN’u olup patolojik GS 7-10, pT2/T3a ve negatif cerrahi marjinliler” olduğu bildirilmiştir(112). Bu sonuçlardan “RP sonucu LN(+) olduğu halde düşük-orta GS’luların, düşük patolojik evrede olanların, negatif cerrahi marjinlilerin” adjuvant RT’den yarar görmedikleri anlaşılmaktadır.
– RP sonrası prostat yatağında nüks, pelvik LN’larında nüks ve retroperitoneal LN’larında nüks vakaları survival açısından farklılıklar göstermektedir. RP + extended LND yapılıp LN(+) gelen 1003 hastada yapılan araştırmada; ortalama 76.7 aylık takipte pN+ olanların ortalama 1/3 ünde klinik nüks geliştiği, RP den sonra BCR gelişenlerden 183 hastada klinik nüks geliştiği(%49.5), iskelet sistemi veya visseral metastaz gelişenlerde kansere özgü mortalitenin diğer metastaz yeri guruplarına göre anlamlı derecede daha yüksek olduğu ve nüks yerinin kansere özgü mortalite yönünden bağımsız prediktör olduğu(s), pelvik bölge yada nodal metastaz gösterenlerin sistemik olmayan tedavilerden daha fazla yarar gördüğü, kemik, visseral organ metastazı gösterenlerin de sistemik tedavilerden daha fazla yarar görebileceği bildirilmiştir(113). Kemik yada visseral organlarda andiferansiye hücrelerin çoğalma kabiliyetinin daha yüksek olabileceği yani bazı organ metastazlarında survival’ın kısa olmasının tümör biyolojisinden ve fenotipinden kaynaklanabileceği belirtilmektedir(113). Bu çalışmaya Sundi D and Schaeffer EM nin yaptıkları editoryal yorumda “ bir dekad önce RP esnasında yada diagnostik PLND esnasında LN(+) liğine rastlandığında hastalığın dissemine(yaygın, sistemik) olarak kabul edildiği” görüşünü hatırlatmaktadırlar(114). Halbuki bu araştırmalar pN+ olan her hastada kanserin sistemik olmadığını göstermektedir. Johns Hopkins’den yapılan araştırmada da 505 pN1 hastada 10 yıllık kansere özgü survival’ın uygulanan tedaviye göre %72-82 arasında değiştiği, sekonder(adjuvan) EBRT yada ADT almayanlarda ise %52 olduğu bildirilmiştir(115). Bu sonuçlardan sonra pN1 olan hastalara ilave tedavi yapılmalı mı yada yapılacaksa ideal zamanlama ne olmalı sorularına cevap vermenin güç olduğu, nodal evrelemenin revize edilmesi gerektiği belirtilmektedir(114).
-RP’de LN(+) bulunan hastalarda klinik nüks gelişmesinin tabii seyri; Lokalize prostat kanserli olup RP ve extended PLN diseksiyonu yapılanların ortalama %10 unda LN pozitifliğine rastlanmaktadır(116,117). RP’de LN(+) olanların seyri farklılıklar göstermektedir, kiminde lenf nodlarının çıkarılmasından sonra hiçbir progresyon olmazken bazlarında biyokimyasal nüks gelişmekte ve klinik nüks gelişebilmektedir. RP de LN(+) olan extended PLN diseksiyonu yapılıp ADT almamış olanlarda uzun süreli takiplerde ortalama %30 unda biyokimyasal nüks gelişmediği belirtilmektedir(118). RP’de LN(+) gelen hastalara adjuvant tedavi başlanması genellikle uygun bulunurken bir kısım otörler hemen başlanmamasını uygun görmektedirler.
-Mayo Klinik’den yapılan araştırmada 1987-2012 döneminde RP yapılıp patoloji sonucunda LN(+) gelen 1011 hastanın ortalama takibinin 17.6 yıl olduğu, 15 yılda klinik nüks oranının %33 ve biyokimyasal nüks oranının %65.9 olduğu, 20 yılda kansere özgü mortalite oranının %31 olduğu, klinik nüks gelişenlerde RP den sonra klinik nükse kadar geçen ortalama sürenin 5 yıl olduğu, biyokimyasal nüks gelişenlerde ise klinik nüks oranının %52 olduğu,
-klinik nüksün prediklerinin “biyopsi GS 8-10 olması, pozitif LN sayısı, patolojik GS’u, cerrahiden sonra geçen yıl olarak süre ve salvage RT ” olduğu, klinik nüksden sonra 15 yılda kansere özgü mortalite oranının %80 olduğu ve klinik nüksden sonra ortalama kansere özgü sağ kalımın 30 ay olduğu bildirilmiştir(119).
–Bu araştırma sonuçlarından da görüleceği gibi RP’de LN pozitif bulunan her üç hastadan birinde 15 yılda klinik nüks gelişmekte olup kalan 2/3 hastada gerek LN diseksiyonunun gerekse bununla birlikte adjuvan tedavilerin sayesinde klinik nüks gelişmemektedir. Biyokimyasal nüks oranı 15 yılda %65.9 olduğu halde klinik nüks oranının %33 olması biyokimyasal nükslülerin ortalama yarısında klinik nüks gelişmediğini göstermektedir. Bu araştırmacıların da belirttiği gibi erken klinik nükslülerde kansere spesifik ölümün yüksek oranda olması o kişideki kanserin biyolojik özellikleriyle ilgili olabileceğine dikkat çekilmiştir(119). Aynı otörler aynı çalışmayı “RP den sonra pN+ prostat kanserlilerin uzun süreli takipte risklerinin belirlenmesi” başlığı ile bir başka dergide yayınlamışlar olup bu çalışma da önceki çalışmadaki (119 nolu çalışmadaki ) verileri bildirip çok değişkenli analizlerde 3 yada daha fazla pozitif LN olmasının, GS 8-10 olmasının, PSM var olmasının kansere özgü mortaliteyi anlamlı derecede arttırdığını, adjuvan RT yapılmasının kansere özgü mortaliteyi anlamlı derecede azalttığını belirtmişlerdir(120). Yine bu çalışmada pN+ hastalarda 20 yılda biyokimyasal nüks, metastaz, kansere özgü mortalite ve tüm sebeplerden mortalite oranlarının sırayla %69, %36, %31 ve %70 olduğu belirtilmiştir(120).
-RP’de LN(+) olan hastalarda erken PSA yükselmesinin klinik nüks ve kansere özgü mortalite ile ilişkisini araştıran bir diğer çalışmada da; RP den 6 hafta sonraki ölçümlerde PSA değeri ≥ 0.1ng/ml vs PSA<0.1 ng/ml olarak hastalar iki guruba ayrıldığında klinik nüks oranının bu guruplarda sırayla 5 yılda %61.3 vs %9.3 ve 8 yılda da %69 vs %11.6 olduğu(s), RP den sonraki erken PSA değerinin prognostik olarak önemli bir parametre olduğu bildirilmiştir(110). RP’de LN(+) gelen hastaların uzun süreli takiplerinde RP sonrası PSA yükselmesi devam edenlerin %80 inde klinik nüks geliştiği belirtilmektedir(110).
-Önceleri RP esnasında froozen’da LN’unda pozitifliğe rastlanması durumunda hastalığın sistemik olduğunu düşünülür ve ameliyata devam edilmezdi. Sonraki araştırmalarda LN(+) gelen böyle hastalarda LND ile birlikte RP nin tamamlanmasının 10 yılda survival’da ortalama %30 iyileşme sağladığı gösterilmiştir(121-123).
-Lenf nodlarındaki metastazın prostattaki kansere göre grade’i, diferansiasyonu bazen farklı olabilmekte ve bazen prostattaki kansere göre daha kötü diferansiasyon gösterebilmektedir. Lenf nodu metastazlarının uzak metastaza dönüşmesinin sebeplerinden birinin bu faktör olabileceği ileri sürülmektedir. M.D. Anderson’dan yapılan çalışmada 200 lenfadenektomi spesmeni vs RP spesmeni ve 100 otopsi spesmeni prostatik kanser diferansiasyon yönünden karşılaştırılmıştır; %73.5 vakada metastaz ile prostattaki kanser aynı grade’de bulunduğu, otopsilerin ise %96 sında prostatla metastazların aynı grade’de olduğu bildirilmiştir(124). 242 vakadan oluşan bir başka çalışmada da %45 vakada lenf nodundaki kanserin GS’unun prostatdaki kanserin GS’undan daha yüksek olduğu, %12 vakada daha düşük olduğu bildirilmiştir(125). Her iki çalışmada da otörler metastazlarda dediferansiasyona meyil olduğunu vurgulamışlardır. RT yapılan 49 hastada da benzer çalışma yapılmış, 49 hastanın 35 inde(%71.4) nüks gelişmiş ve nükslerde grade’in primer grade’den yüksek olduğu belirtilmiştir(126).
6-RP sonucunda pozitif cerrahi marjin (PSM)
-RP’de cerrahi marjinin pozitif gelmesi ilerde klinik nüks yada uzak metastaz gelişmesi risklerini taşıyıp taşımadığı konusu ve PSM’li hastalara hemen adjuvan tedavi başlanması konusu tartışmalıdır. RP spesmeninin patolojik incelenmesinde PSM bulunması kötü (adverse) patolojik göstergelerden biridir. Ancak PSM’nin her zaman metastaza kadar ilerleyen bir süreç olmayabileceği yani bazı hastalarda metastaz için risk oluştururken bazı hastalarda böyle bir risk oluşturmadığı kabul edilmektedir. Eğer PSM ile birlikte diğer kötü (adverse) patolojik göstergeler varsa (SVI, LNI, EPE gibi) adjuvant tedavilere hemen başlanması görüşü ağırlıklıdır, sadece PSM olanlarda öncelikle izlem önerilmektedir.
-RP’den sonra pT2 hastalarda PSM’nin survival’a etkisinin diğer tümör karekteristiklerine bağlı olduğu ileri sürülmüştür(127). RP sonrası PSM yada extraprostatic extention (EPE) biyokimyasal nüks için bağımsız risk faktörleri olarak kabul edilmektedir(128). Sooriakumaran et al 20000 den fazla RP’yi kapsayan international çalışmalarında cerrahi tekniğe bağlı olarak PSM oranının %14-%23 olduğunu bildirmişlerdir(129). Eğer pT2 PSM’li yada pT3 PSM’li yada PSM’siz hastalara RT uygulanacaksa bunun adjuvan mı salvage mı olacağı da tartışmalıdır. Guideline’larda RP sonrası PSM, SVI, EPE gibi kötü patolojik bulguları olan hastalarda adjuvan RT yada izlem önerilmektedir(130,131). Daha önce gerçekleştirilen 3 randomize çalışmada pT3 + PSM’li hastalarda observasyon (izlem) vs RT karşılaştırılmıştır: Bunlar SWOG 8794, EORTC 22911 ve ARO 96-02/AUO AP 09/95 çalışmalarıdır(77,78,80). Bunlardan sadece SWOG çalışmasında bu özellikteki hastalara RT uygulamasının metastazsız survival ve tüm sağ kalım yönünden yarar görüldüğü belirtilmektedir(77). Radikal prostatektomi sonucunda cerrahi pozitif marjinli yada ekstraprostatik yayılımlı hastalarda randomize olarak adjuvan radyoterapi(aRT) versus izlemin etkinliğini araştıran randomize kontrollü Finlandiya çalışmasında; ortalama takibin 9.3 yıl olduğu, 10 yıllık tüm sağ kalımın aRT gurubunda %92 vs izlem gurubunda %87(ns) olduğu, her iki gurupta da Pca’ne özgü 10 yıllık sağ kalımın %100 olduğu(ns), 10 yıllık BRC’süz survival’ın aRT gurubunda %82 vs izlem gurubunda %61(s) olduğu bildirilmiştir(132).
7-Genomik prostat skoru (GPS), Decipher skoru
–“The OncotypeDX Prostate Cancer” polymerase chain reaction(PCR) ile gerçekleştirilen biopsi bazlı bir yöntem olup biopsideki kanser dokusundan ekstrakte edilen RNA’larda 17 geni belirleyerek skorlama yapılan bir değerlendirmedir(133). Sonuçta bu değerlendirmede “Genomic Prostate Score(GPS)” numerik olarak belirlenmekte ve skor 0-100 arasında değerlendirilmektedir. Tümör agressivliği ve kötü prognostik belirtiler arttıkça GPS artmaktadır. Van Den Eeden et al nın “lokalize prostat kanserli olup radikal prostatektomi yapılanlarda metastaz ve prostat kanseri sebebiyle ölümün prediktörü olarak biyopside 17 gen’i baz alan “Genomic Prostate Score”nun önemini araştırdıkları çalışmalarında; tek değişkenli analizlerde GPS ile prostat kanserine bağlı ölüm arasında ve metastaz zamanı arasında anlamlı derecede(s) ilişki bulunduğu, GPS<20 olan düşük yada orta riskli hiçbir hastada metastaz gelişmediği, sonuçta klinik lokalize Pca’li olup RP yapılmışlarda GPS’nin uzun süreli sonuçların bağımsız prediktörü olduğu ve yeni teşhis edilmiş Pca’lilerde risk değerlendirmesinde kullanılabileceği bildirilmiştir(133).
-“Decipher skorlaması ” daha önce tanımlanan 22 genomdan oluşan bir testtir. Decipher skorunun metastaz için bağımsız prediktör olduğu(s), sonuç olarak yüksek Decipher skorunun metastaz gelişimini önceden görebileceği bildirilmiştir(134-136). Bu sebeple yüksek Decipher skorluların erken adjuvan tedaviden yarar görebileceği belirtilmektedir.
8-BRCA mutasyonu: BRCA 1 ve BRCA 2 genleri DNA onarımında rolü olan genlerdir, özellikle BRCA 2 gen mutasyonunda yüksek riskli Pca sıklığının arttığı ve bunun tüm evrelerdeki Pca’leri için prognostik önemi olduğu bilinmektedir. Lokalize Pca için RP olmuş hastalardan BRCA gen mutasyonu olanların daha yüksek oranda metastaz gelişim riski taşıdığı, kansere özgü sağ kalım (CSS) yönünden anlamlı derecede kötü prognoza sahip oldukları ve BRCA gen mutasyonunun kötü prognostik bir gösterge olduğu bildirilmiştir(137).
Lokalize prostat kanserlilerde post-op nüks ve metastaz riskini azaltabilmek için lokal tedavilerde dikkat edilmesi gereken durumlar
-RP yapılacak lokalize prostat kanserlilerde prostatın çıkarılması ile birlikte lenf nodu diseksiyonu yapılacak hastalarda bu işlemin “extended” olarak yapılması hem cerrahi sonrası doğru patolojik evreleme için hem de lenf nodlarında muhtemel rezüdüel tümöral doku kalmaması açılarından önemlidir. Doğru patolojik evreleme için önemli bir faktör de spesmenin örnekleme yöntemi yerine tümünün incelenmesidir (whole mount). Düşük risk gurubunda olan lokalize prostat kanserlilerde bazı cerrahlar PLND yapmamaktadırlar. Bununla ilgili nomogramlar geliştirilmiş olup lenf nodu metastazı riski %5 den az olanlara PLND yapılmayabilmektedir, özellikle robotik RP’lerde bu uygulamaya daha sık rastlanmaktadır. PLNM riski düşük olanlara RP’de PLND yapmayanların bu hastalara neden aktif izlem (AS) uygulamadıkları sorusu akla gelmektedir. Bir diğer önemli husus da RP öncesi hastaların PSMA PET/CT ile değerlendirilmesidir; PSMA PET/CT ile pre-op değerlendirilen bir kısım hastada tedavi kararı değişebilmektedir, konvansiyonal gereçlerle yapılan değerlendirmeye göre PSMA PET/CT ile daha güvenilir sonuçlar alınmaktadır.
– Lokalize prostat kanserlerinde “uzak metastazsız survival’ın (distant metastasis-free survival, DMFS)” tüm sağ kalım (OS) için güçlü bir gösterge olduğu bilinmektedir. Lokal nüksün (local failure) uzak metastazın kaynağı olabileceği kabul edilmekte ve uzak metastazın bir diğer sebebi de lokal tedavi esnasında önceden var olabilen, teşhis edilememiş occult mikroskobik uzak metastazlar olduğu belirtilmektedir. Lokalize Pca için definitif radyoterapi (RT) sonrasında lokal nüks oluşmaması için RT dozunun yüksek olması yada effektiv doz uygulanmasının önemli olduğu kabul edilmektedir. Retrospektif yada randomize çalışmaların sonuçlarına göre kanserin lokal kontrolünün iyi olduğu durumlarda DMFS’nin yükseldiği, Pca’ne özgü survival’ın (PCSS) yükseldiği belirtilmektedir. İki randomize kontrollü çalışmada uzak metastazların ilave ADT uygulanmadan sadece yüksek doz uygulamayla (dose escalation) PCSS’da ve OS’da iyileşme sağladığı belirtilmiştir(138,139). Araştırmaların çoğunda RT ile birlikte ADT uygulanması önerilmektedir. ADT’nin radyasyona duyarlılığı arttırıcı etkisiyle kanserin lokal kontrolünün sağlanabildiği, okkült metastazlar üzerine cytostatic ve cytotoxic etkilerle DMFS’ın iyileştiği belirtilmektedir(140). Kanserin lokal kontrolünün yetersizliğinden kaynaklanabilecek uzak metastazların orta risk gurubu Pca’lerinde yüksek risk gurubu Pca’lerine göre daha düşük olduğu belirtilmektedir(140). Lokalize prostat kanserlerinin RT ile definitif tedavisinde önemli bir konuda da “sadece prostatın ışınlanması yada prostat ile birlikte bölgesel lenf nodlarının da ışınlanması” konusudur. Genel kabul gören kriterlere göre eğer kanser sadece intraprostatik ise ve hasta düşük-orta risk gurubunda ise ve PSMA PET/CT’de lenf nodları ile ilgili şüpheli bir durum yoksa sadece prostatın ışınlanması yeterli olacaktır. Eğer hasta yüksek risk gurubunda ise, PSMA PET/CT’de bölgesel lenf nodlarında şüpheli durum varsa ve/veya SVI yada EPE şüphesi varsa bu durumda prostatın ışınlanması ile birlikte bölgesel lenf nodlarının da ışınlanması ilerde nüks ve metastaz riskini azaltacaktır.
-Ma et al nın “orta ve yüksek risk gurubu Pca’lerinde değişik dozlarda definitif radyoterapi + kısa yada uzun süreli ADT uygulanması sonucunda lokal nüks durumunu” randomize kontrollü çalışma sonuçlarına göre araştırdıkları meta-analiz değerlendirmede ; 6245 hastanın orta risk gurubunda vs 6288 hastanın da yüksek gurubunda olmak üzere toplam 12533 hastanın var olduğu, ortalama takibin 11 yıl olduğu, bu hastaların 1985-2015 dönemine ait hastalar olduğu, yüksek risk gurubu hastalarda lokal nüks, uzak metastaz, PCSM ve tüm sebeplerden ölüm oranlarının sırayla 795(%13), 1288 (%21), 1034 (%16.5) ve 3210 (%51) olduğu, orta risk gurubu hastalarda da lokal nüks, uzak metastaz, PCSM ve tüm sebeplerden ölüm oranlarının sırayla 449 (%7.1), 451 (%7.2), 353 (%5.6) ve 2374 (%38) olduğu, lokal nükssüz hastalarda Pca sebebiyle ölümün lokal nükslülere göre anlamlı derecede düşük olduğu, yüksek risk gurubunda ve orta risk gurubunda yüksek doz RT’nin düşük doz RT’ye göre lokal nüksü anlamlı derecede azalttığı (s), sonuç olarak lokal nüksün yüksek riskli hastalarda OS, PCSS, ve DMFS için bağımsız prognostik faktör olduğu, lokal nüksün orta risk gurubu hastalarda ise DMFS için bağımsız prognostik faktör olduğu, Pca’nin lokal kontrolünün optimal yapılabilmesi durumunda lokal nüks sebebiyle uzak metastaz gelişmesi riskinin azaltılabileceği bildirilmiştir(140).RT sonrası relap-free diyebilmek için PSA değerlendirmesi yada görüntüleme gereçlerinin sonuçları her zaman güvenilir olmayabilmektedir, bazen bu bulgular normal göründüğü halde hasta gerçekte relaps-free olmamaktadır.
– Groen et al “definif RT’den sonra metastaz gelişmesinin önemli sebebinin primer tümör için yetersiz doz RT uygulanmasından kaynaklandığı” hipotezini ileri sürmüşlerdir (141). Groen et al definitif lokal tedavi olarak “EBRT + “simültane focal boost” uygulananlarda standart EBRT uygulananlara göre “local failure-free survival (LFS) ve bölgesel-uzak metastazsız survival ‘ın daha yüksek olduğunu bildirmişlerdir(141).
-Yüksek risk gurubu lokalize Pca’leri için definitif RT uygulamalarında RT + ADT’ne ilave olarak docetaxel de uygulanması çalışmaları yapılmıştır. Bu çalışmaların sonucunda RT + ADT uygulananlarla RT + ADT +docetaxel uygulananlar arasında uzun süreli tüm sağ kalım sonuçlarının benzer olduğu ve docetaxel’in ilave katkı sağlamadığı bildirilmiştir(142-144).
-Prostat kanserinin risk gurubuna göre seçilecek definitif tedavi yöntemi, RT’ye ilave ADT’nin süresi de önemlidir. Agressiv karekterli lokalize prostat kanserlilerde definitiv tedavi olarak RT uygulandığında lokal nüks riski yüksek olmaktadır. Kishan et al Gleason Grade gurup 4-5 lokalize Pca’lilerde definitif RT’den sonra ortalama 6.4 yıllık takipte “ lokal nüks, uzak metastaz, prostat kanserine özgü ölüm (PCSM), tüm sebeplerden ölüm oranlarının sırayla %24, %37, %30 ve %67 “ olduğunu bildirmişlerdir(145). Kishan et al “lokal nüksün tüm sağ kalım, Pca’ne özgü sağ kalım, uzak metastazsız sağ kalım ile anlamlı derecede ilişki gösterdiğini (her biri için p<0.001), lokal nüks gelişmeyenlerde gelişenlere göre PCSM’nin anlamlı derecede daha düşük olduğunu(s), daha uzun süreli ADT’nin daha kısa süreli ADT’ne göre daha yararlı olduğunu” belirtmişlerdir(145).
Lokalize prostat kanserlerinde nüks riskini azaltmak amacıyla radikal prostatektomi öncesi neoadjuvant amaçlı tedavi
Neoadjuvant androjen deprivasyon tedavisi(ADT)
-Klinik olarak yüksek risk gurubu lokalize prostat kanserlerinde RP sonrası nüksü önleyebilmek amacıyla neoadjuvant ADT uygulamaları yapılmaktadır. Önceki yıllarda yapılan “RP öncesi neoadjuvant ADT” uygulamaları ile ilgili meta analiz sonuçlarında; LHRH agonistleri/antagonistleri ilk jenerasyon antiandrojenlerle yapılan uygulamalar
cerrahi sonuçlarda iyileşme göstermesine rağmen hastalıksız sağ kalımda (DFS) ve tüm sağ kalımda (OS) yararı olmadığı bildirilmiştir(146). Yakın zamanda neoadjuvant ADT uygulamalarında yeni jenerasyon androjen reseptör inhibitörleri yada neoadjuvant olarak docetaxel uygulamaları yapılmaktadır. Ryan et al yüksek risk gurubu (HRPC) prostat kanserleri için neoadjuvant tedavinin primer tümörde evre küçülmesi (downstaging) yoluyla negatif cerrahi marjin (NSM) sağladığını ve mikrometastazların tedavisine olumlu katkı sağladığını belirtmişlerdir(147). Lokalize HRPC’lilerde “tek başına RP versus neoadjuvant ADT + docetaxel ve sonrasında radikal prostaektomi” başlıklı faz III çalışmasında tüm sağ kalımda anlamlı derecede iyileşme görülmesine rağmen BCR’süz survival’da anlamlı derecede iyileşme görülmediği bildirilmiştir(148). Ravi et al nın yüksek risk gurubu lokalize prostat kanserlilerde “yeni neoadjuvant hormonal terapiyi (NHT) takiben radikal prostatektomi versus doğrudan radikal prostatektomi sonuçlarının karşılaştırmalı analizini” yaptıkları retrospektif çalışmalarında metastazsız survival’ın (MFS) NHT + RP gurubunda anlamlı derecede (s) daha uzun olduğunu, 3 yıllık MFS’ın sırayla %96 vs %68 (s) olduğunu, aynı sırayla 8 (%7) vs 63 (%24) hastanın adjuvant radyoterapi (RT) aldığını, salvage tedavi oranlarının da aynı sırayla %34 vs %46 olduğunu bildirilmişlerdir(149).
– Yüksek risk gurubu lokalize prostat kanserlilerde randomize neoadjuvant ADT’nin sonuçlarının araştırıldığı faz II çalışmada hastaların RP öncesi 1:1 oranında 6 siklus “apalutamid, abirateron asetat, prednizon, leuprolide” (gurup I) vs “abirateron, prednizon, leuprolide” (gurup II) randomize edildiği, PSM oranlarının gurup I ve II de sırayla %7.3 vs %12 olduğu, tümör volümünün tüm hasta gurubunda %91 azaldığı, mpMRI daki tümör volümü ile patolojik tümör volümü arasında zayıf korelasyon olduğu bildirilmiştir(150).
-McKay et al neoadjuvant olarak enzalutamid+leuprolid+abirateron kombinasyonunda patolojik komplet cevap oranının %30 vs enzalutamid +leuprolide uygulamalarında %16 olduğunu bildirmişlerdir(151).
Yüksek risk gurubu-çok yüksek risk gurubu lokalize prostat kanserlilerde lokal tedavi ADT’den sonra metastaz riski ve bu tedavilerin sonuçları
-Literatürde birden çok yüksek risk (HR) ve çok yüksek risk (VHR) kriteri tanımlanmıştır. Briganti et al HR kriterlerini “pT2 PSM’li, pT3a GS≥4+3, pT3b, LN(+) GS≥3+4, bunlardan biri var olanlar” olarak belirtmişlerdir ve bunlarda 5 yılda BCR riskin ortalama %50 olduğunu, nüks ve Pca sebebiyle ölüm riskinin yüksek olduğunu belirtmişlerdir(152). NCCN (National Comprehensive Cancer Network©) tanımına göre yeni teşhis edilmiş klinik lokalize prostat kanserlerinin %17-%31 nin yüksek risk gurubu (HR) olduğu belirtilmekte ve yüksek riski kriteri “GS 8-10 yada PSA> 20 ng/ml veya klinik evre T3” olarak tanımlanmaktadır(153,154). NCCN kriterlerine göre HR hastaları kendi içinde HR vs VHR olarak sınıflandırmamıştır. Johns Hopkins (JH) Üniversitesinin yüksek risk ve çok yüksek risk kriterleri NCCN kriterlerinden bazı farklılıklar arzetmektedir; JH sınıflamasına göre NCCN’nın HR gurubu kanserleri içinde JH sınıflamasına göre %85 nin HG (cT3a veya Gleason Grade Gurup IV/V yada PSA > 20 ng/ml kriterlerinden en az 1 tanesinin var olması) ve %15 nin çok yüksek risk gurubunda (VHR) olduğu belirtilmektedir. JH tanımlamasına göre VHR kriterleri “cT3b-cT4 ve/veya primer Gleason grade-pattern 5 ve/veya 2-3 HR kriterinin var olması ve/veya Gleason Grade Gurup IV/V, 5 yada daha fazla pozitif core var olması” kriterlerinden en az birinin var olması) olarak belirtilmiştir(155,156). JH kriterleri kullanıldığında VHR hastalarında HR hastalarına göre daha kötü onkolojik sonuçlar (biyokimyasal nüks-BCR, metastazsız sağ kalım-MFS, kansere özgü mortalite-CSM yönlerinden ) olduğu belirtilmiştir(156,157).
-JH gurubunun 2010-2016 döneminde kendi kriterlerine uyan HR ve VHR hastalarda RP vs RT uygulamalarının survival’a etkisini araştırdıkları Chierigo et al nın çalışmalarında; tüm hastaların NCCN kriterlerine göre HR gurubunda olduğu, JH kriterlerine göre bu hastaları HR ve VHR olarak değerlendirdikleri, genel olarak tüm gurupta(HR + VHR) RP vs RT uygulananlarda 5 yıllık kanser spesifik mortalite (CSM) oranlarının sırayla %2.3 vs %4.1 (s) olduğu, NCCN kombine gurupta RP’nin EBRT’ye CSM açısından üstün olduğu, JH kriterlerine göre bu üstünlüğün VHR gurubunda olduğu, HR gurubunda RP vs EBRT arasında CSM yönünden anlamlı farklılık olmadığı bildirilmiştir(158). Bu sonuçlardan yüksek veya çok yüksek risk gurubu lokalize prostat kanserleri için definif tedavi olarak RP’nin CSM, metastazsız sağ kalım yönlerinden RT’ye göre daha üstün olduğu görülmekte ve JH gurubuna göre bu üstünlüğün özellikle VHR gurubunda olduğu belirtilmektedir. Knipper et al ve Tilki et albiyopsi GS 9-10 hastalarda RP vs EBRT uygulanmasında CSM’nin RP uygulananlarda EBRT uygulananlara göre daha iyi olduğunu bildirmişleridir(159,160).
-Lokalize yüksek risk gurubu yada lokal ileri evre Pca’lilere EAU guideline’da multimodal yaklaşım önerilmektedir. Bu multimodal yaklaşımlar; extended PLND’u ile birlikte RP + post-op RT(ADT) yada 76-78 Gy EBRT, EBRT + brakiterapi(BT) + uzun süreli ADT(10 yıldan fazla ömür beklenenlere) olarak sunulmuştur(161). Histolojik olarak lokalize yüksek risk gurubu olduğu kanıtlanmış (ISUP kategorizasyonuna göre Grade Gurup 4-5 yada GS 8-10 veya PSA > 20 ng/ml, yada klinik evre
lokal-ileri evrede olan(herhangi bir PSA değeri ile birlikte cT3-4 yada cN+, herhangi bir ISUP kategorisinde)Pca’lerinde primer tedavinin risk ve faydalarının analiz edildiği review çalışmada; RP vs EBRT+ADT karşılaştırmasında uzak metastazsız survival yönünden anlamlı fark olmadığı ancak tüm sebeplerden ölüm(OM) ve Pca’ne özgü ölüm(PCSM) yönünden RP’nin daha iyi sonuçlar verdiği, RP vs RP + EBRT +ADT karşılaştırmasında tüm sağ kalımın (OS) kombine gurupta daha üstün olduğu, tek başına RP vs EBRT+BT+ADT karşılaştırıldığında da tek başına RP gurubunda daha yüksek OM ve PCSM görüldüğü, EBRT vs EBRT +BT karşılaştırıldığında kombinasyonun onkolojik sonuçlar açısından daha üstün olduğu,lokal ileri evre Pca’lerinde onkolojik sonuçlar açısından RP vs EBRT
ADT karşılaştırmasında RP’nin daha üstün olduğu, EBRT
ADT nin tek başına EBRT’ye göre daha üstün olduğu bildirilmiştir(162). Sonuçlardan da görüldüğü gibi lokalize yüksek risk gurubu veya lokal ileri evrede kombine yaklaşımlar (multimodal terapi) tekli yaklaşımlara göre tüm sebeplerden mortalite (OM) ve PCSM yönlerinden daha iyi sonuçlar sağlamaktadır.
– Cerrahi sonuçlarına göre LN metastazı varsa BCR riski %69 a kadar ulaşmakta ve daha yüksek patolojik evrede, daha yüksek GS’unda, PSM durumunda uzun süreli takiplerde kansere özgü ölüm ve tüm sebeplerden ölüm riski artmaktadır(120). Bu gurup hastalarda BCR gelişmeden önce RT ve/veya ADT yapılıp yapılmaması, kemoterapiye erken başlanılıp başlanılmaması tartışılan durumlardır. Çoğunluğu orta risk gurubunda olan ve bir kısmı da yüksek risk gurubunda olan RP yapılan hastalarda kötü (adverse) patolojik göstergelerin (PSM, SVI, EPE) ameliyat sonrası metastaz gelişimine etkilerinin araştırıldığı Ross et al nın çalışmasında; 3809 hastanın verilerinin analiz edildiği, RP den sonra 10 yılda biyokimyasal nüks ve metastaz oranının sırayla %13 ve %6 olduğu, metastaz gelişiminin prediktörlerinin GS ve patolojik evre olduğu, tüm hasta gurubunun %43 ünde kötü patolojik gösterge(PSM, SVI, EPE) var olduğu ve bunların çoğunun pT3 evrede olduğu, kötü patolojik göstergesi olanlarda RP sonrası 10 yılda metastazın kümülatif sıklığının %7.5 olduğu, biyokimyasal nüks gelişenlerde nüksden sonra 5 yılda metastaz gelişim sıklığının %38 olduğu, bu sonuçlara göre orta-yüksek risk gurubunda olan ve RP spesmeninde kötü patolojik göstergeleri olan hastalardan bazılarına hemen ilave RT gerekmeyebileceği bildirilmiştir(163).
-Metastatik olma riski yüksek bir kısım hastada lokal tedavilerin Pca sebebiyle ölüm riskini azalttığı görülürken bir kısmında ise yeterince yararlı olamadığı, kür sağlanamadığı görülmektedir. Bu durumda metastatik olma riski yüksek hangi hastalarda lokal tedavinin yararlı olacağı, hangi hastalarda yarar sağlamayacağı sorusu akla gelmektedir. Literatürde klinik olarak lokalize prostat kanserli bir hastada RP den önce kemik iliğinde yayılmış tümör hücreleri varsa bunların sonradan belirgin metastaza dönüşmesi riskinin 5 kat arttığı, fakat bu hücrelerin RP’den sonra belirgin metastaza dönüşmesi riskinin artmadığı, bunun sebebinin de intact primer lezyonun(kanserli prostatın) vücutta kalmasının metastaz riskini arttırdığı yorumları vardır(164-166). Başlangıçta PSA > 50 ng/ml olan hastalarda metastatik Pca riskinin, yaygın hastalık riskinin yüksek olduğu kabul edilmektedir(167).
-Retrospektif çalışmalarda da muhtemelen occult metastazı olan vakalardan (PSA>50 ng/ml yada N+ vakalar) cerrahi uygulananlarda sadece sistemik tedavi uygulananlara göre survival avantajı olduğu bildirilmiştir(118,168,169). Sooriakumaran et al nın “başlangıçta radikal tedavi yada sadece androjen deprivasyon tedavisi görmüş yaygın hastalık riski yüksek prostat kanserlilerde survival’ı araştırmak” amacıyla İsveç’den yaptıkları çalışmalarında; 1996-2010 döneminde yüksek riskli hastalardan 17602 sine ADT, 630 una RT ve 120 sine de RP yapıldığı, ortalama 15 yıl takip edildiği, sadece ADT alanlarda Pca sebebiyle ve diğer sebeplerle ölüm oranlarının %51 ve %25, radikal tedavi alanlarda ise bu oranların sırayla %11 ve %9.1 olduğu(s), subgurup analizlerde PSA> 100 ng/ml olanlarda Pca sebebiyle ölümün sadece ADT alanlarda radikal tedavi alanlara göre 3 kat yüksek olduğu, PSA 50-100 ng/ml olanlarda Pca sebebiyle ölüm oranının sadece ADT alanlarda ve radikal tedavi alanlarda benzer olduğu(ns), M1/Mx hastalarda da Pca sebebiyle ölüm oranının iki gurupta benzer olduğu(ns)bildirilmiştir(167).
– Cooperberg et al’nın çalışmasında lokalize Pca’li 7538 hastada EBRT ile RP karşılaştırılmış, çok yüksek risk gurubu hastalarda Pca’ne özgü mortalitenin(PCSM) EBRT uygulananlarda RP yapılanlara göre artmış olduğu belirtilmiştir(170). Zelefsky et al da klinik evre cT1-T3a RP yapılmış 1318 hastaya ve EBRT uygulanmış 1062 hastaya ait sonuçlarında; yüksek riskli(HR) olup RP yapılanlarda metastatik progresyonun ve prostat kanserine özgü mortalitenin(PCSM nin) EBRT yapılan HR’li hastalara göre daha düşük olduğunu bildirmişlerdir(171). Yüksek risk gurubu hastalarda ilk tedavi stratejisi olarak RP + PLND önerilmekte, gerektiğinde de salvage tedaviler önerilmektedir.Pompe et al “ 1992-2016 döneminde RP yapılan yüksek risk gurubu (HR) hastalarda ve çok yüksek risk gurubu (VHR) hastalarda PCSM ve tüm sağ kalımı (OS)” araştırmışlardır. VHR olanlarda 5 ve 8 yıllık prostat kanseri sebebiyle mortalitesiz survival’ın (PCSM’siz) %91.9 ve %87 olduğunu, yine VHR gurupta 5 ve 8 yıllık tüm sağ kalımın %85.7 ve %76.1 olduğunu, HR gurupta ise 5 ve 8 yıllık PCSM’siz survivalın %96.1 ve %93.2 olduğunu, 5 ve 8 yıllık tüm sağ kalımın ise %91.5 ve %83.7 olduğunu bildirilmişlerdir(157). Cooperberg et al “Pca’lerinin çoğunun ilk teşhiste düşük yada orta riskli olduğunu, Amerikan erkeklerinde teşhis edilen Pca’lerinin %30 nun yüksek grade’li olduğunu ve bunlarda progresyon ve mortalite riskinin yüksek olduğunu” belirtmişlerdir(153).
-Altmış yaşından genç yüksek grade’li lokalize prostat kanserli hastalarda primer tedavi olarak radikal prostatektomi versus radyoterapinin (± brakiterapi) kansere özgü mortaliteye etkisini araştıran retrospektif çalışmada “ 1459 hastaya (%65.5) primer tedavi olarak RP vs 769 hastaya da(%34.5) RT uygulandığı, 5 ve 7 yıllık Pca’ne özgü mortalite oranlarının RP gurubunda %2.2 ve %4.9 vs RT gurubunda %8.2 ve %12.1(s) olduğu, subgurup analizlerde kansere özgü mortalite açısından EBRT ve EBRT + brakiterapi(BT) gurupları arasında anlamlı fark olmadığı, Pca’ne özgü mortalite ve tüm sebeplerden mortalite açısından RP ile EBRT + BT görenler arasında anlamlı fark görülmediği belirtilmiştir(172). Wallis et al nın review-meta analiz çalışmasında da yüksek grade’li hastalarda RP vs RT karşılaştırıldığında RP yapılanlarda RT yapılanlara göre tüm sebeplerden mortalite ve Pca’ne özgü mortalite sonuçlarının daha iyi olduğu(s) belirtilmiştir(173). GS 9-10 kanserli 1809 hastada EBRT + BT + ADT alanlarda vs RP ve EBRT + ADT uygulananlara göre 7.5 yıllık takipte daha düşük kansere özgü mortalite ve daha düşük tüm sebeplerden mortalite görüldüğü(p=0.001 ve p=0.03) bildirilmiştir(76,174).
– Kibel et al nın “lokalize Pca için RP, EBRT ve brakiterapi uygulananlarda survival ve Pca’ne özgü mortaliteyi” araştırdıkları retrospektif çalışmalarında; 1995-2005 arasında 6485 i RP, 2264 ü EBRT ve 1680 i de brakiterapi (BT) görmüş lokalize Pca’li toplam 10429 hastanın verileri değerlendirilmiştir. RP, EBRT ve brakiterapi görenlerde 10 yıllık Pca’ine özgü mortalite oranının sırayla %1.8, %2.9 ve %2.3 olduğu, Pca’ine özgü mortalitenin EBRT gurubunda RP’ye göre anlamlı derecede yüksek olduğu(s) ancak EBRT ve brakiterapi arasında fark olmadığı(ns), sonuçta RP nin diğer 2 tedavi yöntemine göre küçük oranda fakat anlamlı derecede daha yüksek tüm sağ kalım ve kansere özgü sağ kalım yönünden üstün olduğu bildirilmiştir(175). Birçok diğer çalışmalarda da RP nin EBRT’ye karşı Pca’ine özgü mortalite ve tüm sağ kalım yönünden üstün olduğu bildirilmiştir(171,176-178). Bu sonuçlardan da görüldüğü gibi yüksek risk gurubu lokalize Pca’lilerde lokal tedavi olarak sadece RP uygulananlarda sadece EBRT uygulananlara göre daha düşük Pca’ne özgü mortaliteye (CSM) rastlanmaktadır, ancak EBRT + brakiterapi uygulanması ile sadece RP uygulanmasının CSM açısından benzer sonuçlar verdiği görülmektedir.
Metastatik hormona duyarlı prostat kanserlilerde lokal tedavinin survival’a katkısı
-Metastatik hormona duyarlı prostat kanserlilerden (mHSPC) lokal tedaviden “ilk teşhiste metastatik olan, daha önce prostata yönelik RP veya RT tedavisi görmemiş hastalara RP veya RT yapılması” kastedilmektedir. Daha önce prostattaki kanser için RP veya RT görmüş ve sonradan metastaz gelişmiş hastalar kastedilmemektedir. mHSPC’li seçilmiş hastalara lokal tedavi olarak RP ve RT dışında brakiterapi, metastaz direkt terapiler (MDT), bazen de salvage fokal tedaviler de uygulanabilmektedir. Araştırmalarda bu tedaviler arasında oligometastatik özellik taşıyanlara prostata RT uygulanması en sık uygulanan lokal tedavidir. mHSPC’lilerde hemen daima lokal tedavi ile birlikte ADT, pelvik lenf nodlarına RT de uygulanmaktadır. Metastatik prostat kanserleri bir süre sonra kaçınılmaz olarak kastrasyon rezistant (CRPC) safhaya geçmektedir yani kür sağlanamamaktadır. İlk teşhiste metastatik olarak tespit edilen Pca’lerinde 5 yıllık survival’ın %28 olduğu belirtilmektedir(179). Connor et al oligometastatik prostat kanserlerinde radikal tedavi uygulamaları için “kür sağlamayan radikal tedaviler” tabirini kullanmışlardır(180).
-Ürologların mHSPC’lilerin yönetimi yada bunlara uygulanabilecek tedavilerle ilgili görüşlerini yansıtan veriler “The Advanced Prostate Cancer Consensus Conference (APCCC) 2019 ve 20221 raporlarında” yayınlanmıştır. Bu raporlarda metastatik hormona duyarlı prostat kanserinin yönetimi ile ilgili olarak kesin konsensus’a varılan kararlarda; primer tümörün lokal tedavisinin sadece düşük volümlü (M1)metastazı olan hormona duyarlı kanserlilere tüm sağ kalım (OS) yönünden yararlı olacağı,
– yeni teşhis edilmiş düşük volümlü metastatik hormona duyarlı prostat kanserli hastaların çoğunda RT ile lokal tedavinin yararlı olacağını panelistlerin %84 ü uygun bulurken %16 sı RP’yi uygun bulduğu, mHSPC’li ve cN1 hastalarda prostatın radyoterapisi ile birlikte pelvik lenf nodlarının da ışınlanması gerektiği, mHSPC’lerdeprimer tümör için RP’nin yararı hakkında şimdiye kadar yapılan çalışmalardan bir sonuç yada kanaat oluşmadığı,
-oligometastatik HSPC tanımı için tam bir konsensus oluşmadığı, ilk teşhiste metastazların yeri ve sayısının, metastazların metakranöz yada senkranöz olmasının önemli olduğu,
-tedavi görmemiş de novo oligometastatik Pca’lerinde tedavi kararı vermede metastazın sadece LN’larında olanlarla(uzak LN’ları da dahil) diğer yerlerde(kemik yada visseral organlarda) olmasının ayırımının önemli olduğu, senkranöz oligometastatik HSPC’lerinde “STOPCAP meta-analiz çalışması ve STAMPEDE çalışması” sonuçlarına göre primer tümörün tedavisi + sistemik tedavinin yararlı olduğu, diğer bir tedavi yöntemi olarak metakranöz oligometastatik HSPC’lerinde “sistemik tedavi + tüm lezyonlar için lokal tedavi SABR (stereotactic ablative body radiotherapy)” uygun olduğu belirtilmiştir(1,181). Panelde yeni teşhis edilmiş metastatik hormona duyarlı prostat kanserlerini tanımlamak için “hormona sensitiv, noncastre, castration naive, castration sensitive” gibi aynı anlama gelecek farklı tanımlar kullanıldığı, bunlardan hangisinin en uygun olduğu konusunda konsensus sağlanamadığı belirtilmiştir.
Yeni teşhis edilmiş metastatik hormona duyarlı Pca’lerinde (mHSPC) lokal tedavi olarak radyoterapi
-Metastatik hormona duyarlı Pca’lerinde standart tedavi ADT olup ADT için uygulanan ajanlar da büyük çoğunlukla LHRH agonistleridir. Guideline’larda da belirtildiği gibi son yıllarda mHSPC’lerinde ADT ile birlikte yeni jenerasyon androjen reseptör inhibitörleri (abirateron, enzalutamid, apalutamid yada benzerleri) yada ADT + docetaxel kemoterapisi uygulanması ile sadece ADT uygulanmasına göre survival’da daha iyi sonuçlar alınmıştır.
Metastatik hormona duyarlı prostat kanserlilerde primer tümör için yani prostattaki kanser için radyoterapi uzun süredenberi uygulanan bir tedavi yöntemi değildir ve sonuçları da tam olarak belirli değildir. Bu konuda yapılmış iki geniş serili araştırma STAMPEDE (182,183) ve HORRAD (184) çalışmalarıdır. HORRAD çalışmasında mHSPC’lilerde “ADT vs ADT + prostat için RT” uygulamalarında prostata RT yapılmasının tüm sağ kalımda (OS) ilave yarar sağlamadığı, ancak PSA için progresyon süresini uzattığı belirtilmiştir. STAMPEDE çalışmasında da prostattaki kanser için RT uygulamasının tek başına ADT’ye göre OS’a katkı sağlamadığı belirtilmektedir. Metastatik hormona sensitiv prostat kanseri için radyoterapinin etkinliği “STAMPEDE ve HORRAD çalışmalarının review-meta analizi yapılarak ” “A STOPCAP” review, meta-analiz çalışmasında yapılmıştır (185). Değerlendirmeye alınan hasta sayısı 2118 olup bunlardan HORRAD çalışmasında 2004-2014 döneminde 432 hastanın var olduğu ve ortalama takibin 47 ay olduğu, STAMPEDE çalışmasında da 2013-2016 döneminde 1694 hastanın olduğu ve ortalama takibin 41.9 ay olduğu, her iki çalışmadaki hastaların ortalama yaş, WHO/ECOG performans durumlarının, GS≥8 oranının benzer olduğu, HORRAD çalışmasındakilerin tümünde vs STAMPEDE çalışmasındakilerin %89 da kemik metastazı var olduğu belirtilmiştir. İki gurupta 2126 hastanın global değerlendirilmesinde 969 ölüm olduğu, ADT’ne ilave prostata RT uygulamasının survival’a katkısı olmadığı(ns), progresyonsuz survival’a(PFS) katkısı olmadığı(ns),
-metastaz sayısı 5 den az ve 5 yada daha fazla olarak guruplandırıldığında metastaz sayısı 5 den az olanlarda 3 yılda survival’da mutlak iyileşmenin %7 daha iyi olduğu(s),
-mHSPC’lerinde prostata RT uygulamasının 3 yılda biyokimyasal progresyonda %25-%36 oranında anlamlı iyileşme sağladığı, STAMPEDE gurubunda %4 hastada şiddetli mesane toksisitesi ve %1 şiddetli akut barsak toksisitesi görüldüğü bildirilmiştir(185).
-STAMPEDE çalışmasında düşük metastatik kitleli hastalar “4 den az kemik metastazı olması ve bunlarda kemik metastazının vertebra ve pelvisle sınırlı olması, visseral metastaz olmaması” olarak tanımlanmıştır(183). Literatürde düşük metastatik kitleli Pca yerine “oligometastatik kitleli Pca “ tabiri de kullanılabilmektedir. Oligometastatik tabiri ilk defa Hellman and Weichselbaum tarafından 1995 de kullanılmıştır(186). Lezyonların yeri ve sayısı ile ilgili tam bir tanım yoktur. Konvansiyonel tetkik yöntemlerine göre oligometastatik kabul edilen bir hastada yeni görüntüleme tekniklerine göre daha fazla metastaz tespit edilebilmektedir. Düşük metastatik kitleli hastalarda anlamlı derecede iyileşme “failure-free survival’da” ve “tüm sağ kalımda iyileşme” olarak belirtilmiştir. Taneja SS “bu çalışmanın ürolojik onkoloji topluluğunda tartışmalara yol açacağını ve provakatif bir çalışma olduğunu, bu çalışmanın sonucuna dayanarak metastatik kitleli hastalarda cerrahi uygulanabileceği sonucunun çıkarılmaması gerektiğini, diğer bir ifadeyle bunlara RT uygulanması yerine RP uygulanmasının doğru yaklaşım olmayacağını belirtmiştir(187).
– Ranasinghe et al “metastatik hormona duyarlı prostat kanserlerinde primer tümörün tedavisi” ile ilgli olarak; yüksek volümlü metastatik hormona duyarlı prostat kanserlerinde başlıca tedavi opsiyonlarının “ADT, kemohormonal tedavi (ADT + kemoterapi), ADT + yeni jenerasyon androjen reseptör inhibitörleri (abiraterone, enzalutamide yada benzerleri)” olduğunu, düşük volümlü metastazı olanlarına ADT ile birlikte prostata radyoterapi yapılabileceğini, mHSPC’lerinde HORRAD çalışmasında prostat için RT + ADT vs sadece ADT uygulandığını, bu çalışmada da örnek çapının dar olması, yüksek volümlü metastazların seçilmiş olması, ortalama PSA nın 142 ng/ml olması gibi eleştiriler yapıldığını, sonuçta RT + ADT nin ortalama 47 aylık takipte tüm sağ kalıma yararı olmadığını belirtmişlerdir(188). Ranasinghe et al M1a hastalarda “cytoreductive prostatecmy (CRP)” ile ilgili olarak “CRP’nin tüm sağ kalım ve kansere özgü sağ kalım yönünden RT’den, brakiterapiden ve cerrahi olmayan tedavilerden üstün olarak göründüğünü, mHSPC’lilerde CRP çalışmalarının retrospektif özellikte olduğunu, metastazların volüm ve yerlerinin belirgin olmadığını, konvansiyonel radyolojik yöntemlerin(kemik sintigrafisi, CT gibi) kullanılmış olmasının sonuçlar üzerinde tartışma yarattığını” belirtmişlerdir(188).
– Bu verilerden sonra hem AUA hem de EAU guideline’larında da düşük metastatik kitleli hormona duyarlı prostat kanserlilerde ADT’ne ilave olarak prostata RT uygulanmasının önerildiği belirtilmektedir(189). STAMPEDE çalışmasının uzun süreli sonuçlarında da “ortalama takibin 61.3 ay olduğu, düşük metastatik kitleli hastalarda prostata RT uygulanması + ADT nin sadece ADT’ne göre survival’ın anlamlı derecede daha iyi olduğu, yüksek metastatik kitlesi olanlarda prostata RT uygulanmasının survival’a katkı sağlamadığı” bildirilmiştir(190).
Metastatik hormona duyarlı prostat kanserlilerde lokal tedavi olarak radikal prostatektomi
-Yakın zamanda metastatik Pca’lerinde lokal tedavi uygulanmalarının survival’a anlamlı derecede katkısı olduğunu bildiren çalışmalar bulunmaktadır(191-194). Bu gurup hastalara RP yapılmasının yararı “tümörün ana kaynağı çıkarılarak metastaz gelişimine neden olan cytokine salgılanmasının elimine edildiği” tarzında izah edilmektedir(195,196). Bir başka yorum da “Pca’de metastazların metastatik kaynaklardan kendi kendine geliştiği, bir anlamda yeni metastazların ana kaynaktan değil metastatik kaynaklardan geliştiği” olarak belirtilmiştir(197). Oligometastatik yada düşük volümlü metastazı olan hastalara yapılan radikal prostatektomiye cytoreductive RP(CRP) denmektedir. Sitoredüktif cerrahinin böbrek, kolon, göğüs, over gibi organların kanserlerinde bazı seçilmiş hastalarda yararı tartışmalı olmakla birlikte kısmen yararlı olduğu kabul edilmektedir. Metastatik HSPC’lilerde CRP’nin yararlı olup olmadığı bilinmemektedir. Prostat kanserinde yaygın uygulamaya göre definitif tedaviler klinik olarak organa sınırlı kanseri olan ve 10 yıl yada daha fazla hayat beklentimiz olan Pca’lilere uygulanmaktadır. Konvansiyonel görüntüleme yöntemlerinde belirgin metastaz tespit edilemeyen bir kısım hastalarda, özellikle lokal ileri evre Pca’lilerde çok büyük ihtimalle mikrometastazlar olabileceği kabul edilmekte ve tedavi planlamaları buna göre yapılmaktadır. Konvansiyonal görüntüleme gereçleri ile yapılan araştırmalarda metastaz tespit edilemeyen yada düşük oranda metastaz tespit edilen birçok hastada yeni nesil görüntüleme gereçleri ile, örneğin PSMA PET/CT ile, metastaz tespit edilmektedir. Debulking cerrahinin yani cytoreductive cerrahinin bazı kanserlerde bile (örneğin renal cell cancer’de) yararı tartışmalıdır. Oligometastatik tanımı üzerine de tam bir konsensus bulunmamaktadır.
– Metastatik HSPClilerde RP’nin lokalize hastalara uygulanan RP’ye göre daha riskli olduğu, EPE, PSM gibi kötü patolojik sonuçların çoğu zaman kaçınılmaz olduğu, post-op inkontinans riskinin ve per-op komşu organ yaralanmaları riskinin yüksek olduğu malumdur. Ayrıca bu hastalara RP sonrası ilave tedavi olarak çok yüksek ihtimalle RT ve/veya ADT de gerekecektir. Bu gurup hastalarda RP sonrası metastazlarda muhtemelen bir gerileme olmayacaktır, çünkü hastalık sistemik hale gelmiştir. Bu sebeplerle metastatik Pca’lilere RP’nin bir yarar sağlayıp sağlamayacağı şüphelidir, yarar sağlamayacağı kanaati daha yaygındır. Böyle hastalarda sadece ADT uygulanması da ADT ile birlikte ilave tedavilerin (yeni jenerasyon AR inhibitörleri, docetaxel, prostata RT uygulanması) uygulanmasına göre survival açısından daha az yarar sağlamaktadır. ADT‘nin kanser hücrelerinde apoptozis etkisi vardır. Apoptozis ADT’ne ilave olarak yapılacak radyoterapiye kanser hücrelerini daha hassas hale getirmektedir yani radyoterapinin etkinliğini arttırmaktadır. Bu sebeple PSMA PET/CT ile metastazların sınırlı sayıda olduğu tespit edilen mHSPC’lilere RP yerine RT uygulanması daha rasyonel yaklaşım görünmektedir.
-Oligometastatik(5 yada daha az kemik metastazı olan, LN’larında metastaz olan yada olmayan, visseral organ metastazı olmayan) 11 prostat kanserlide açık RP ve extended LND nun 5 yıllık sonuçlarını bildiren Gandaglia et al nın çalışmalarında; ortalama takibin 63 ay olduğu, 7 yıllık klinik progresyon ve kansere özgü survival oranlarının %45 ve %82 olduğu bildirilmiştir(198). Bu çalışmada pre-op ortalama PSA nın 11.4 ng/ml olduğu, 3 hastanın klinik evre cT1, 5 hastanın cT2 ve 3 hastanın da cT3 olduğu, biyopsi GS nun bir hastada <6 (metastatik bir hastada GS nun 6 dan düşük olması ilginçtir), 3 hastada GS 7 ve 7 hastada GS nun 8-10 olduğu, 5 hastada kemik metastazından biyopsi yapıldığı belirtilmektedir(198). Çalışmanın verilerinden anlaşıldığı üzere bu gurup hastalarda cerrahi uygulama sırasında ve post-op dönemde ciddi güçlükler(kan kaybının yüksekliği, anastomoz kaçağı, grade 3 komplikasyonlar) olmuştur. Böyle bir uygulamanın eleştirilebilecek birçok yönü vardır. Oligometastatik HSPC’lilerde RP yapılabileceğini savunanlar “lokal tümör kitlesinin çıkarılmasıyla sistemik tediviye cevabın artacağını” ileri sürmektedirler. Literatür bilgilerinde metastatik olup RP yapılanlarda metastatik olup da RP yapılmayanlara göre onkolojik sonuçların daha iyi olduğu belirtilmiştir(191,199). CRP nin survival’a katkısı olduğunu bildiren çalışmaların çoğunun sistemik tedavi ile karşılaştırmalı ve retrospektif olduğu, hasta seçiminde bias’lar olduğu, sağlık durumu daha iyi olan, düşük metastatik kitleli ve asemptomatik hastaların CRP gurubuna alındığı eleştirileri yapılmaktadır(200).
-Oligometastatik hastalarda CRP’nin sonuçlarını bildiren Steuber et al nın araştırmasında çalışma gurubu düşük volümlü metastazı olan (sadece 1-3 kemik lezyonlular) 43 hastadan oluşmakta ve kontrol gurubu da sistemik terapi alan 40 hastadan oluşmaktadır. CRP yapılanların rezektabl tümörler(≤cT3) olduğu, ilk teşhisteki PSA nın 150 ng/ml yada daha düşük olduğu, hastaların daha önce RT almamış oldukları, tüm hastalara kontinü ADT yada maksimal androjen blokajı uygulandığı, kastrasyon rezistant prostat kanseri (CRPC) gelişmeden hiçbir hastanın kemoterapi almadığı,
-CRP yapılan gurubun daha genç(s), daha düşük PSA’lı(s), daha düşük evreli(s) ve daha az kemik metastazlı(s) oldukları ve biyopsi GS’larının benzer olduğu(ns), CRP yapılanlarda ortalama takibin 32.7 ay vs sistemik terapi alanlarda ise 82.2 ay olduğu, iki gurup arasında kastrasyon rezistant free survival ve tüm sağ kalım yönünden anlamlı farklılık olmadığı(ns), sonuç olarak CRP’nin onkolojik sonuçlar açısından yararlı olmadığı, çalışmalarında ana limitasyonunun CRP gurupta takip süresinin kısa olduğunu bildirilmiştir(200).
– Sooriakumaran et al nın çok merkezli retrospektif araştırmalarında da; ilk teşhiste metastatik Pca(M1) olup RP ve extended LND yapılan 106 hastada ortalama PSA nın 23.5 ng/ml olduğu, hastaların %42.5 inde pre-op LN metastazı ve %66 sında da kemik metastazı tespit edildiği, post-op PSA ölçümü yapılmadığı, ortalama GS nun 8.5 olduğu, PSM oranının %53.8 olduğu, ortalama takibin 22.8 ay olduğu ve bu sürede %88.7 sinin sağ olduğu ancak bu ortalama takip süresinde 12 hastanın Pca sebebiyle öldüğü ve bu ölen hastalarda ilk teşhiste iskelet metastazı var olduğu, RP den 90 gün sonra kontinans oranının %55.7 olduğu bildirilmiştir(201).
– Heidenreich et al “düşük volümlü kemik metastazı olan, visseral metastaz yada yaygın LN metastazı olmayan mHSPC’li 23 hastada (gurup I) CRP sonuçları ile bazal özellikleri benzer olan ve ADT uygulanan 38 hastanın (gurup II)” sonuçlarını karşılaştırmışlardır(202). Gurup I ve II de ortalama takibin 34.5 ay vs 47 ay olduğu, kastrasyon rezistant oluncaya kadar geçen ortalama sürenin gurup I ve II de sırayla 40 ay ve 29 ay(s) olduğu, gurup I ve II de klinik progresyonsuz survival’ın 38.6 ay vs 26.5 ay(s) olduğu, kansere özgü survival oranlarının guruplarda sırayla %95.6 vs %84.2(s) olduğu ve tüm sağ kalımın benzer olduğu(ns), iyi seçilmiş vakalarda, uzun ömür beklenenlerde “cytoreductive” RP yapılabileceği bildirilmiştir(202). Bu sonuçlardan mHSPC’lilerde “cytoreductive RP” yapılmasının mHSPC’li olup da RP yapılmayanlara göre kastrasyon rezistant safhaya geçiş süresini uzattığı, bu açıdan yararlı olduğu anlaşılmaktadır. Metastatik Pca’lilerde RP yapılmasıyla ilgili yukarda verilen araştırmaların hemen hepsinde de ortalama takip süreleri oldukça kısa olup hiçbirinde de RP den sonra metastazlarda gerileme yada kaybolma ile ilgili bilgi verilmemektedir.
-Metastatik hormona duyarlı Pca’lilerde lokal tedavinin (LT) survival’a etkisiyle ilgili Bannurah et al nın çalışmalarında da; 474 metastatik Pca’liye lokal tedavi uygulandığı(313 üne RP, 161 ine RT), lokal tedavi uygulanmayan(NLT) 1896 hastanın sonuçlarıyla kansere özgü mortalite(CSM) yönünden karşılaştırma yapıldığı, çok değişkenli analizlerde LT uygulananlarda NLT yapılanlara göre daha düşük CSM bulunduğu(s), risk kriterleri(yaş, ırk, biyopsi GS, klinik evre, LN metastazı ve metastatik substage) arttıkça LT’nin etkisinin azaldığı, CRP yapılanlarda kanser sebebiyle mortalitenin (CSM’nin) RT yapılanlara göre daha düşük olduğu, en düşük CSM oranının GS≤7, ≤cT3 ve M1a hasta gurubunda olduğu bildirilmiştir(203). Bu çalışmada da bir çok limitasyon(çalışmanın retrospektif olması, hastaların comorbidite-performans durumunun belirtilmemesi, PSA değerleriyle ilgili bilgi eksikliği gibi) bildirilmiş olup yukarda yapılan eleştiriler bu çalışma için de geçerlidir.
– Satkunasivam et al retrospektif çalışmalarında “2004-2009 döneminde SEER verilerine göre tespit edilen 4069 metastatik Pca’liden 47 sine RP, 88 ine RT(IMRT) ve 107 sine de conformal RT yapıldığını vs 3827 sine hiçbir lokal tedavi yapılmadığını, ortalama takibin 20 ay olduğunu, Pca’ine özgü mortaliteyi hiçbir lokal tedavi yapılmayanlara göre CRP’nin %52 azalttığını ve IMRT nin %62 azalttığını, buna karşılık conformal RT nin hiçbir lokal tedavi uygulamamaya göre Pca’ine özgü mortaliteyi etkilemediğini” bildirilmişlerdir(204). Takipte 2872 ölüm olduğu, bunların 2058 inin(%72) Pca inden öldüğü belirtilmiştir. Üç yıllık tüm sağ kalımın RP yapılanlarda %73, IMRT yapılanlarda %72, conformal RT yapılanlarda %37 ve hiçbir lokal tedavi yapılmayanlarda da %34 olduğu belirtilmişitir.3 yıllık kansere özgü sağ kalımın ise bu guruplarda sırayla %79, %82, %49 ve %46 olduğu belirtilmiştir.
-Metastatik prostat kanserlerinde lokal tedavinin(radikal prostatektomi, prostat için radyoterapi, brakiterapi ± ADT) survival’a etkilerini araştıran çalışmada; National Cancer Data Base(NCDT) verilerinin baz alındığı, 2004-2012 döneminde teşhis edilen metastatik Pca’li 15501 hastanın değerlendirmeye alındığı, lokal tedavi olarak teşhisten sonra 6 ay içinde uygulanan CRP, brakiterapi ve/veya EBRT(±ADT) nin kastedildiği, 1470 hastaya lokal tedavi uygulandığı(%77 sine EBRT, %20 sine CRP ve %3 üne de brakiterapi) ve CRP uygulananların %79 una PLND da uygulandığı, lokal tedavi uygulanmayanlara ADT, bekle-gör(WW) yada prostat dışı bölgelere EBRT uygulandığı, ortalama takibin 39 ay olduğu,
-lokal tedavi uygulanan hastaların “daha genç hastalar, daha düşük PSA değeri olan hastalar, kötü diferansiye kanserin daha az olduğu hastalar, ilerlemiş N evresinin daha az olduğu hastalar, komorbiditenin(CCI’nin) daha düşük olduğu hastalar” olduğu, lokal tedavi uygulananlarda 3 yıllık “tüm sebeplerden mortalitesiz survival’ın” lokal tedavi uygulanmayanlara göre daha yüksek olduğu(%69 vs %54, s), lokal tedavi uygulanmayanlarda yaş ve Charlson komorbidite indeksinin tüm sebeplerden mortalite için anlamlı prediktör olduğu, bu prediktör risklerin artmasıyla lokal tedavinin tüm sebeplerden mortaliteyi azaltıcı yada iyileştirici etkisinin azaldığı, daha az agressiv tümörü olan ve genel sağlık durumu iyi olan metastatik Pca’lerinde lokal tedavinin yararlı olduğu bildirilmiştir(205).
–Culp et al tarafından yapılan retrospektif araştırmada; 2004-2010 döneminde “the American Joint Committee on Cancer, AJCC” evrelemesine göre(206) evre IV M1a-c olan 8185 Pca’li hastadan(%5.9 u M1a, %70 I M1b, ve %24.1 I de M1c) 7811 hastaya lokal tedavi yapılmadığı(non local treatment gurup), 245 ine CRP yapıldığı(CRP gurup), 129 una brakiterapi yapıldığı(BT gurup),
-daha önce RT, krioterapi, TUR-P yapılanların değerlendirmeye alınmadığı, ortalama takibin 16 ay olduğu, total 3115 hastanın (%38.1) Pca sebebiyle öldüğü, bu ölümlerin lokal tedavi yapılmayan gurupta %40.7, CRP gurubunda %13.5 ve BT gurubunda %26.4 olduğu, 5 yıllık tüm sağ kalımın CRP ve BT guruplarında lokal tedavi yapılmayan guruba göre anlamlı derecede yüksek olduğu( guruplarda sırayla %67.4, %52.6 ve %22.5, s), RP ve BT guruplarında kansere özgü survival’ın lokal tedavi yapılmayan guruba göre anlamlı derecede yüksek olduğu(sırayla %75.8, %61.3 ve %48.7), kanser dışı sebeplerle ölen 1284 hastada(%15.7) survival yönünden guruplar arasında anlamlı farklılık bulunmadığı,
-sonuçta mHSPC’lilerin bazılarının lokal definitif tedaviden yararlanabileceği bildirilmiştir(191). Bu çalışmanın prospektif olmaması, ortalama takibin 16 ay gibi oldukça kısa olması başta olmak üzere pek çok eleştirilebilecek yönleri bulunmaktadır. Hiçbir guideline’da da metastatik Pca için RP veya BT uygulanmasına dair öneri yoktur. Ayrıca Culp et al nın çalışmasında bu gurup hastalara ADT uygulanıp uygulanmadığı hakkında da bilgi yoktur.
– Thompson et al daha önce lokal tedavi görüp sonradan metastaz gelişen hormone sensitiv hastalarla vs ilk teşhiste metastatik olan hormone sensitive hastaları ADT’den yararlanma yönünden karşılaştırmışlardır; daha önce RP veya RT görenlerde Pca sebebiyle ölüm riskinin ilk teşhiste metastatik olanlara göre anlamlı derecede daha az olduğunu (s) bildirilmişlerdir(207). Gratzke et al da 1998-2010 döneminde metastatik Pca’li hastalardan 1538 hastaya RP yapılmış olduğunu (beraberinde sistemik terapi yapılıp yapılmadığı belirtilmemiştir), analizlerinde önceden RP yapılmış olanlarda tüm sağ kalımın %55 vs RP yapılmamış olanlarda ise %21 olduğu bildirilmiştir(208).
Metastatik hormona duyarlı prostat kanserlilerde diğer tedavi seçenekleri
I- Chemo-hormonal tedavi
-Metastatik hormona duyarlı Pca’lerinde (mHSPC) standart tedavi ADT olup bunlarda 5 yıllık survival’ın %30 olduğu, ortalama 3 yılda hormona dirençli hale dönüştüğü yani kastrasyon rezistant Pca (CRPC) geliştiği belirtilmektedir(209). mHSPC’lerinde gerek kemohormonal tedavinin gerekse ADT + yeni jenerasyon androjen reseptör inhibitörlerini uygulamanın temel amacı CRPC gelişimini geciktirebilmek, dolayısıyla survival’ı uzatabilmektir.
– mHSPC’lilerde standart ADT’ne docetaxel eklenmesinin tüm sağ kalım açısından tek başına ADT’ne göre yararlı olduğunu bildiren birçok çalışma vardır (CHAARTED, GETUG-AFU15, STAMPEDE)(182,210,211). Avrupa Üroloji Kongresinde Sweeney et al nın sunumunda ise bu özellikteki hastalarda ADT’ne ilave docetaxel’in(D) sadece ADT’ne göre tüm sağ kalıma yararının sadece yüksek volümlü metastazı olanlarda görüldüğü(visseral metastazlılarda, en az biri vertebrada ve pelvis dışında 4 yada daha fazla kemik metastazı olanlarda), düşük volümlü metastazı olanlarda görülmediği bildirilmiştir(212). Bir diğer meta analiz çalışmasında da ADT’ne D eklenmesinin 4 yılda tüm sağ kalımda %9 iyileşme sağladığı bildirilmiştir(213). Gravis et al nın sonuçlarına göre kemo-hormonal tedaviye yüksek volümlü metastazı olanlarda erken başlamanın yararı olduğu görülmektedir(214). Şüphesiz ki yüksek volümlü metastazı olan Pca’lilerde erken kemo-hormonal tedaviden hedeflenen amaç CRPC gelişmesini geciktirebilmektir.
-Metastatik prostat kanserlilerde ADT’de yada kemo-hormonal tedavide testosteronun (T) kastre seviyeye düşürülebilmesi ve düşüş hızı tedavinin olumlu yada olumsuz gidişinin bir göstergesi olabilmektedir. ADT gören prostat kanserlilerde testosteron seviyesinin kastre düzeye hızlı yada yavaş düşüşünün prognoz açısından önemi tartışmalıdır. Tam bir konsensus olmamakla birlikte ADT’ne başladıktan sonra T seviyesinin hızla kastre seviyeye düşüşünün prognoz açısından daha iyi olduğu kabul edilmektedir. ADT gören ve %65 i T3 yada daha yukarı evre olan T1c-T4 225 hastada ortalama takip süresinin 45.8 ay olduğu, hastaların %23.1 ine birkaç kurs ADT den sonra docetaxel kemoterapisi verildiği, ortalama nadir PSA seviyesinin 0.04 ng/ml olduğu, ortalama nadir testosteron(T) seviyesinin 6 ayda 13ng/dl olduğu, çok değişkenli analizlerde “metastazın, nadir PSA nın, nadir PSA ya erişim süresinin” progresyonsuz survival ile anlamlı ilişki gösterdiği, tüm sağ kalım yönünden nadir T seviyesi olarak 20ng/dl ye erişim 6 aydan kısa ve 6 aydan uzun olanlar arasında anlamlı farklılık olmadığı(ns), bu sebeple prognoz için kritik faktörün T seviyesinin hızlı düşüşü değil T seviyesinin düşmesi olduğu bildirilmiştir(215).
-mHSPC’lilerde gerçekleştirilen CHAARTED çalışmasında ADT’ne ilave 6 siklus docetaxel(75 mg/m2 ) uygulamasıyla chemohormonal gurupta sadece ADT alanlara göre survival açısından 13.6 aylık iyileşme görüldüğü(57.6 ay vs 44 ay, s) bildirilmiştir(210). STAMPEDE çalışmasında da mHSPC’li hastalar 4 guruba ayrılmışlar: sadece ADT, ADT + docetaxel, ADT + zoledronat, ADT + docetaxel + zoledronat uygulananlar. Chemohormonal tedavi ayağında survival açısından sadece ADT alanlara göre 10 aylık iyileşme olduğu(81 vs 71 ay, s) bildirilmiştir(182). GETUG-AFU 15 çalışmasında ise chemohormonal tedavi gurubu sadece ADT alanlarla karşılaştırılmış ve sonuçlarda anlamlı farklılık olmadığı, ancak post hoc analizlerde yüksek volümlü hastalık olanlarda kemo-hormonal tedaviyle ölümlerde %20 azalma(ns) olduğu bildirilmiştir(211,216).
– Metastatik hormon tedavisi almamış Pca’lilerde ADT’ne ilave olarak androjen reseptör hedefli ilaçların yada docetaxel uygulanmasının hangisinin daha yararlı olabileceği tam olarak bilinmemektedir, daha doğrusu survival’a benzer derecede katkı sağladıkları düşünülmektedir. Hormon tedavisi almamış (hormone naive) yüksek risk gurubu metastatik prostat kanserlerinde abirateron asetat +ADT vs docetaxel + ADT nin sonuçlarıyla ilgili meta-analiz, review çalışmada; 6067 hastanın sonuçlarının değerlendirildiği, 1181 hastanın(%19.5) D+ADT, 1557 hastanın (%25.7) AA+ADT ve 3329 hastanın da(%54.9) sadece ADT aldığı,
-tüm sağ kalım yönünden D+ADT alanlarla vs AA+ADT alanlar arasında anlamlı fark görülmezken bu her iki gurubun sadece ADT alanlara göre tüm sağ kalım yönünden anlamlı derecede üstünlük gösterdikleri(s), Bayesian ve SUCRA analizlerde first line tedavi olarak AA+ADT nin tercih edildiği bidirilmiştir(217).
II-ADT + yeni jenerasyon androjen sentez inhibitörleri ile tedavi
-Yeni jenerasyon androjen sentez inhibitörleri olarak “abiraterone asetate, enzalutamide, darulotamide, apalutamide” sayılabilir. Abiraterone asetat (AA) “cytochrome P-450 CYP17 enzimini” bloke ederek steroidlerden androjen üretimini testislerde, adrenalde ve prostat içinde inhibisyonu yoluyla etki gösteren androjen reseptör antagonisti bir ajandır. Kemoterapi öncesi ve sonrasında kullanılabilmektedir. Neoadjuvan olarak ADT + abiraterone + prednizon kombinasyonunun yeni teşhis edilmiş yüksek risk gurubu lokalize Pca’lerinde ADT’ne rezistant klonlar oluşmadan önce tümör kitlesini küçülttüğü belirtilmektedir(209). STAMPEDE çalışmasında yeni teşhis edilmiş metastatik, LN(+) yada yüksek riskli lokal-ileri evre hastaların ya tek başına ADT’ne yada ADT + abirateron 1000mg + prednizon 5mg tedaviye randomize edildikleri, kombinasyon gurubunda 3 yıllık tüm sağ kalımın tek başına ADT’ne göre daha iyi olduğu(s), ölüm riskinin relatif olarak %37 azaldığı(s), tedavi başarısızlığı riskinin %71 azaldığı(s) bildirilmiştir(218). Çok merkezli faz III LATITUDE çalışmasında da; yeni teşhis edilmiş mHSPC’li hastaların ADT + abiraterone + prednizon vs tek başına ADT’ne randomize edildikleri, 3 yılda kombinasyon gurubundaki hastaların 2/3 nün vs sadece ADT gurubundakilerin yarısının sağ olduğu(s), kombinasyon gurubunda radyografik progresyonsuz survival’ın daha iyi olduğu(s) ve %53 risk azalması görüldüğü(s) bildirilmiştir(219).
–Guideline önerileri:
-Gerek 2019 gerekse 2021 APCCC (Advanced Prostate Cancer Concensus Conference) kararlarında tüm metastatik Pca’leri için genetik test/genetik danışmanlık yapılmasını uygun bulunmuştur. Bu öneri AUA/SUO 2023 guideline’da da yapılmıştır(220).
– AUA/SUO 2023 guideline önerilerinde sağlıklı mHSPC’lilere intermittant ADT genellikle önerilmemektedir. Panelde ilk teşhiste (de novo) mHSPC olanlara ADT + docetaxel yada ADT + abiraterone acetate + prednisone veya ADT + darulotomide önerilmiştir(strong öneri, abirateron veya docetaxel için grade A öneri, darulotimide için grade B öneri)(220).
-mHSPC’leri için AUA/ASTRO/SUO 2020 önerilerinde de; metastazların yerinin, sayısının, metastazların düşük yada yüksek volümlü olmasının önemi vurgulanmakta, bu guruptaki hastalarda semptom olup olmamasının prognoz açısından önemli olduğu, kemik ağrısı olanlarda 10 yıllık survival’ın daha kısa olduğu, bunlarda yapılan gen analizlerinde %11.8 de DNA onarım genlerinde germ-line mutasyon olduğu ve germ-line mutasyonu olan hastalarda PARP inhibitörlerinin kullanılmasının yada sitotoksik kemoterapiye erken başlanmasının uygun olacağı belirtilmektedir(2,3). ADT ile birlikte apalutamid için TITAN çalışmasında, enzalutamid için ENZAMED çalışmasında, docetaxel için CHAARTED çalışmasında tek başına ADT + plaseboya karşın daha üstün, olumlu sonuçlar alındığı belirtilmiştir. ADT uygulanmaksızın tek başına nonsteroidal antiandrojen tedavisi uygulanmaması gerektiği belirtilmiştir.
III-Metastaz direkt terapi (MDT)
-Bu başlık altında aşağıda verilen sonuçların bir kısmı ilk teşhiste metastatik olan hastalara yapılan MDT sonuçlarını, bir kısmı da definitif tedavi sonra nüks yada metastaz gelişen hastalara yapılan MDT sonuçlarını yansıtmaktadır. Bu farklı hasta guruplarına ait MDT sonuçlarını birlikte vermemizin amacı MDT’nin etkinliği ile ilgili genel değerlendirme yapılmasını sağlamak amaçlıdır.
-“Metastasis-directed thearpy, MDT” genellikle sınırlı lenf nodu metastazlarına uygulanan bir tedavi yöntemidir. PET/CT kullanımının artması metastatik lezyonların daha erken teşhisini kolaylaştırmıştır, bu sebeple oligometastatik hastalık teşhis oranı da artmıştır. AUA guideline’da metastatik kastrasyona duyarlı Pca’leri için spesifik bir MDT belirtilmemiştir(2), EAU guideline’da sadece LN’larına invazyon olması halinde salvage LND önerilmiştir(221). MDT’nin standart ADT’ne göre onkolojik açıdan daha yararlı olduğu belirtilmektedir(99).
-Nodal nükslerin tedavisi olarak ADT, elective nodal radyoterapi (ENRT), sterotactic body radyoterapi (SBRT, SABR), salvage LND gibi değişik alternatif yaklaşımlar vardır. Radikal tedavilerden sonra LN’larında düşük volümlü hastalık nüksü görülen Pca’lilerde ENRT ve SBRT’nin metastazsız survival yönünden, etkinlik ve toksisite oranlarının karşılaştırılmasını amaçlayan retrospektif araştırmada; 3 yıllık metastazsız survival’ın(MFS) SBRT gurubunda %68 vs ENRT gurubunda %77 (s) olduğu, çok değişkenli analizlerde sadece 1 LN’da metastazı olanlarda ENRT uygulamasının SBRT uygulamasına göre daha uzun MFS sağladığı (s), birden fazla LN metastazı olanlarda MFS yönünden iki gurup arasında anlamlı fark olmadığı (ns), lenf nodlarında hastalığın progresyonunun SBRT uygulananlarda ENRT uygulananlara göre daha yüksek olduğu(s), kemik metastazı, prostat yatağında metastaz ve visseral metastazın iki gurupta benzer olduğu, total nüksün SBRT gurubunda daha yüksek olduğu(s), 3 yıllık “kastrasyon rezistant Pca(CRPC) free survival’ın” iki gurupta benzer olduğu(ns), ENRT gurubunda toksisitenin SBRT gurubuna göre daha yüksek olduğu, bu araştırmada ADT’nin etkisi hakkında yorum için verilerin yetersiz olduğu(inconclusive) bildirilmiştir(222).
-Andrews et al nın radikal prostatektomi yada radyoterapi sonrasında “solitary oligorecurrent” prostat kanserlerinde ADT uygulanmadan MDT uygulanan hastalarda yaptıkları çalışmada MDT uygulanan 124 soliter oligorekürrent hastanın sonuçlarının değerlendirildiği, bunlardan 67 hastaya MDT olarak cerrahi uygulandığı ve 57 hastaya da MDT olarak SABR uygulandığı, MDT uygulanmadan önce bu 124 hastadan 115 hastaya primer tedavi olarak RP, 8 hastaya EBRT ve 1 hastaya da brakiterapi uygulanmış olduğu, MDT olarak cerrahi uygulananlarda ortalama takibin 55.2 ay olduğu, 31 hastada (%46) komplet PSA cevabı alındığı,
-MDT olarak SBRT(SABR) uygulanan 57 hastada MDT’den sonra ortalama takibin 53.4 ay olduğu, 57 hastadan 11 hastada (%19) komplet PSA cevabı sağlandığı,
-takiplerde cerrahi olarak MDT uygulanan 67 hastadan 62 hastada (%92.5) BCR geliştiği ve bunlarda radyografik progresyon için geçen ortalama sürenin 14.9 ay olduğu ve 3 yıllık radyografik progresyonsuz survival oranının %29 olduğu,sonuçta 67 hastadan 57 hastada (%85.1) radyografik progresyon geliştiği,
-MDT olarak SBRT uygulanan 57 hastada BCR için geçen ortalama sürenin 9.5 ay olduğu, 3 yıllık biyokimyasal nükssüz survival oranının %12.3 olduğu, sonuçta 57 hastadan 54 hastada (%94.7) BCR geliştiği, radyografik progresyon için geçen ortalama sürenin 12 ay olduğu, 3 yıllık radyografik PFS’ın %16.5 olduğu ve sonuçta 57 hastadan 50 hastada (%87.7) radyografik progresyon geliştiği bildirilmiştir(223).
-Andrews et al nın çalışmasının sonuçlarına göre MDT olarak cerrahi uygulananlarda SBRT uygulananlara göre daha yüksek oranda komplet PSA cevabı alınmasına rağmen (%46 vs %19), 3 yıllık biyokimyasal nükssüz survival’ın birbirine yakın olduğu (%17.9 vs %12.3), takiplerde cerrahi uygulanan vs SBRT uygulanan hastalarda nihayetinde BCR gelişmesi oranlarının benzer olduğu (%92.5 vs %94.7), radyografik progresyon gelişme oranlarının benzer olduğu (%85.1 vs %87.7), sistemik tedaviye geçiş oranlarının (%77 vs %87) ve sistemik tedaviye geçiş sürelerinin (18.5 ay vs 17.8 ay) benzer olduğu, CRPC gelişmesi için geçen ortalama sürenin de benzer olduğu (54 ay vs 50.4 ay) görülmektedir. Bu çalışmada tek metastazı olan hastalara MDT uygulandığı halde sonuçlar tam tatmin edici olmamıştır yada kürabl olmamıştır. Andrews et al nın çalışmasındaki sonuçlar sistemik tedavi uygulanmaksızın doğrudan MDT yapılan hastalara ait sonuçlardır. Eğer oligometastatik hastalara MDT uygulanacaksa bunlarda MDT ile birlikte sistemik tedavi uygulamak daha olumlu sonuçlar verebilir.
-Fossati et al çok merkezli çalışmalarında MDT olarak salvage LND (sLND) yapılan hastalarda 3 yıllık MFS’ın ortalama %50 olduğunu belirtmişlerdir(98). Bleser et al ise kendi araştırmalarında bu oranın %71 olduğunu belirtmektedirler(222).
-Oligometastatik Pca’lilerde “stereotactic ablative body radiotherapy, SABR” nin etkinliğini araştıran bir başka çalışmada da 33 hastada 50 metastatik lezyona SABR (SBRT) uygulandığı, 1 ve 2 yıllık lokal progresyonsuz survival’ın %97 ve %93, 1 ve 2 yıllık progresyonsuz survival’ın %58 ve %39 olduğu, SABR süresince 22 hastanın ADT’ni almadığı bildirilmiştir(224). Uygulamanın emniyetli, kısa süreli sonuçların tatmin edici olduğu bildirilmesine rağmen sonuçlar çok başarılı görünmemektedir. Metastazlı prostat kanserlerinde bir kısım hastada belirlenebilen metastaz sayısı düşük olsa da bunlarda belirlenememiş mikrometastazların var olması ihtimali oldukça yüksektir.
-Glicksman et al nın “ oligorecurrent” prostat kanserlerinde “metastasis-directed therapy” ile ilgili çalışmalarında araştırmaya “maksimal lokal tedavi görmüş (RP ve post-op RT görmüş)”
ve PSMA PET/CT/MR de “oligorecurrent” durum tespit edilmiş” hastaların dahil edildiği, nükslerin hastaların %92 de lenf nodlarında ve %8 de kemiklerde olduğu, MDT olarak 27 hastaya SBRT ve 10 hastaya cerrahi(pelvik LND ve retroperitoneal LN diseksiyonu) uygulandığı, ortalama takibin 15.9 ay olduğu, ortalama 7.7 ayda 8 hastada komplet biyokimyasal cevap alındığı(5 cerrahi ve 3 SBRT uygulanan hastalar), 10 hastada parsiyel cevap alındığı (PSA nın %50 den fazla azalması), PSA progresyonu için geçen ortalama sürenin 17.7 ay olduğu bildirilmiştir(225).
-Boeri et al nın kemik yada lenf nodunda oligometastazı olan hastalarda MDT çalışmasında lenf nodu metastazı olanlarda olumlu sonuçlar alınırken kemik metastazlılarda survival açısından olumlu sonuçlar alınmadığı bildirilmiştir(226).
-Bu sonuçların genel analizi yapıldığında RP’den sonra LN nükslerinde sLND veya SBRT uygulanması yerine ENRT ile birlikte simültane integre boost(sib) uygulamasının daha yararlı olduğu ve cerrahiye göre daha az morbiditeli olduğu, çünkü PET/CT ile oligorekürrent hastalık olarak kabul edilen birçok durumda PET/CT nin gerçekte var olan başka LN metastazlarını tespit edemediği, RT uygulamasında da hedefin sadece nükslü LN yerine o bölgedeki LN’larının komplet ışınlamasının uygun olacağı, SBRT uygulamasında bunun yapılmadığı, RT birlikte ADT uygulamasının RT’nin etkinliğini arttırabileceği, özellikle birden fazla LN metastazı olanlarda ve primer tedavi öncesi yüksek risk gurubunda olanlarda lenf nodlarının bölgesinin ışınlanması ile birlikte prostat yatağına da RT uygulanmasının ilerde gelişebilecek lokal nüksler açısından koruyucu olabileceği kabul edilmektedir.
Daha önce lokal tedavi almamış kastrasyon rezistant prostat kanserlilerde lokal tedavi (!)
-Daha önce lokal tedavi almamış ve kastrasyon rezistant safhaya gelmiş prostat kanserleri “ilk teşhis edildiğinde metastatik olan ve teşhis edildikten sonra hormonal tedavi yada kemo-hormonal tedavi uygulanmış ve nihayetinde kastrasyon rezistant duruma dönüşmüş” hastalardır. Bu hastalar muhtemelen ilk teşhis edildiklerinde metastatik yada lokal-ileri evrede yada lokalize olduğu halde radikal tedaviler yerine hormonal tedavinin tercih edildiği hastalardır.
– AUA/ASTRO/SUO 2020 guideline önerilerinde kastrasyon rezistant prostat kanserleri için “öncelikle metastatik olmayan CRPC’leri (nmCRPC’leri) ve metastatik CRPC’leri (mCRPC’leri)” olarak guruplandırılması gerektiği,
-nmCRPC’leri için FDA tarafından kabul edilmiş spesifik bir tedavi ajanı olmadığı, ADT ile birlikte AR inhibitörleri uygulamalarının vs ADT + plaseboya göre metastazsız survival açısından (MFS) yarar sağladığı, PSADT 10 aydan kısa olanlarda yani metastaz riski yüksek olanlarda ADT’ne ilave olarak AR inhibitörleri (apalutamid, enzalutamid, darolutamid gibi) önerildiği, bu öneride SPARTAN (apalutamid için), ARAMIS (darolutamid için) ve PROSPER (enzalutamid için) çalışmalarının sonuçlarının dikkate alındığı, FDA tarafından nmCRPC’leri için kabul edilmemiş (onay verilmemiş) kemoterapi, immünoterapi yada diğer ajanların kullanılmasının kesinlikle önerilmediği, bunlarda ADT devam edilmesi gerektiği yada izlem uygulanabileceği,
-mCRPC’leri için de rutin radyografik görüntülemeler yapılması gerektiği(sadece PSA sonucu ile takibin değerlendirilmesinin yetersiz olacağı), ADT hiç kesilmemesi gerektiği ve beraberinde abirateron, enzalutamid, docetaxel tedavilerinin uygulanmasının doğru olacağı, asemptomatik yada minimal semptomatiklere spuleucel-T uygulanabileceği, bundan başka kemik metastazlılara radium-223 uygulanabileceği,
–daha önce ADT + abirateron docetaxel yada ADT
docetaxel yada ADT
enzalutamid tedavisi görmüş olup progresyon gelişenlere cabazitaxel uygulanabileceği, bunlarda abirateron uygulanalarda enzalutamide geçiş yada enzalutamid uygulananlarda abiraterona geçiş yerine cabazitaxel uygulanmasının CARD çalışması sonucunda daha olumlu görüldüğü,
–enzalutamid yada abirateron uygulamalarında progresyon görülenlerde PARP inhibitörleri(özellikle BRCA 1/2, ATM mutasyonu olanlarda) kullanılabileceği belirtilmiştir(2,3).
-Kastrasyon rezistant durum “ nadir PSA’nın %25 yükselmesi ya da 0.2 ng/ml nin üzerinde ardışık iki PSA artışı“ olarak tanımlanmaktadır, universal bir PSA artış tanımı bulunmamaktadır(227). nmCRPC’lilerden PSAD 10 ay olanlarda metastaz gelişmesi riski yada Pca sebebiyle ölüm riski yüksektir(228).
-Metastatik Pca’lerinde uygulama pratiğinde genelde kemoterapien önce AR’lerinin inhibisyonunu hedefleyen tedaviler tercih edilmektedir. Bu tercihte kemoterapinin toksisitelerinden çekinmenin rolü olabileceği belirtilmektedir. AR hedefli tedavilerde “cross-resistance” (bir diğerine direnç gelişmesi) belirgindir. Abiraterona direnç gelişenlerde enzalutamid’e geçilince alınan cevap zayıf olmakta yada enzalutamide direnç gelişenlerde abirateron’a geçilince alınan cevap zayıf olmaktadır(229). Örneğin mCRPC’li olup PSA progresyonu gelişinceye kadar abirateron alan ve ondan sonra enzalutamid’e geçilen hastalarda yada tersi uygulananlarda ikinci AR hedefli tedaviden sonra PSA progresyonuna kadar geçen ortalama sürenin her iki tercihte de 3 aydan kısa olduğu bildirilmiştir(229). mCRPC’lilerde uygulamalarda AR hedefli tedaviye erken direnç geliştiğinde taxane gurubu kemoterapi uygulanmasının yararının ikincil bir androjen reseptör hedefli tedaviye göre daha üstün olduğu belirtilmektedir(230).
-CARD çalışmasında daha önce docetaxel tedavisi almış ve 12 ay içinde progresyon geliştiğinde alternatif olarak AR hedefli tedavi(abiratreon yada enzalutamid) almış mCRPC’li 255 hasta randomize tarzda 1:1 oranında cabazitaxel versus abirateron veya enzalutamid uygulaması (önceden abirateron almışsa sonradan enzalutaid yada tam tersi) emniyet ve etkinlik yönünden radyografik progresyon gelişinceye kadar karşılaştırılmıştır. Cabazitaxel alanlarda radyografik progresyonsuz survival’ın (rPFS) abirateron yada enzalutamid alanlara göre anlamlı derecede daha uzun olduğu, cabazitaxel’in ölüm riskini anlamlı derecede %36 oranında azalttığı bildirilmiştir(231). Ayrıca cabazitaxel’in ağrıya cevabı anlamlı derecede iyileştirdiği (%45 vs %19.3, s), ağrı progresyonu için geçen süreyi uzattığı da belirtilmiştir. Randomize çalışmalarda da kemoterapi almamış mCRPC’lilerde abirateron veya enzalutamid kullanımında ortalama PSA progresyonsuz survival’ın her iki ajan için de 8 aydan kısa olduğu belirtilmiştir(229,232-235).
-Klinik uygulamalarda genellikle AR hedefli tedavilerden birine direnç geliştiğinde diğerine başlanmaktadır. Ancak CARD çalışması daha önce docetaxel tedavisi almış, devamında AR hedefli tedaviye başlanmış, 12 ay içinde AR hedefli tedaviye direnç gelişenlerde diğer bir AR hedefli ajan yerine cabazitaxel uygulanmasının daha üstün olduğunu göstermiştir.
Daha önce lokal tedavi almamış CRPC’lilerde RP(!)
-Önceki yıllardaki RP uygulamalarında pre-op klinik olarak pozitif LN olanlar, lokal-ileri evrede olanlar çoğu zaman inoperabl kabul edilirlerdi. Daha ötesi “klinik lokalize kabul edilip RP yapılanlarda operasyonda frozen esnasında pozitif LN sonucu gelenlerde” operasyon sonlandırılırdı ve daha sonra sadece ADT veya RT ± ADT alternatifleri değerlendirilirdi. Son yıllarda kemik metastazı olmayan sınırlı pozitif LN olanlara, lokal-ileri evrede olanlara RP yapıldığı, yakın zamanda da seçilmiş metastatik Pca’lilere de RP yapıldığı görülmektedir. Şimdi olay bir adım ileri götürülmüş olup daha önce RP yapılmamış metastatik kastrasyon rezistant prostat kanserlilere de (mCRPC) RP yapıldığına rastlamaktayız. Prostat kanseri için RP yapmada temel amacın hastanın survival’nı uzatmak olduğu malumdur. Metastatik hormona duyarlı Pca’lilerde (mHSPC) RP’nin survival’a ne kadar katkı sağladığı belirli değildir. Gerek mHSPC’lilerde gerekse mCRPC’lilerde RP yapmayı savunanlar “prostatın çıkarılmasıyla primer tümörün immünsupressiv etkisinin ortadan kalkacağını, lethal clone’ların ve onların sisteme(dolaşıma) geçişinin ortadan kalkacağını, lokal progresyon morbiditesinin ortadan kalkacağını, performans durumu iyi hastalarda lokal progresyon semptomlarının azalacağını” savunmaktadırlar(236,237).
-Literatürde daha önce lokal tedavi görmemiş mCRPC’leri için RP uygulanması ile ilgili fazla bilgi bulunmamaktadır. mCRPC’lerinde RP sonuçlarının bildirildiği Reichard et al nın çalışmasında; 2008-2016 döneminde 14 mCRPC’liye RP yapıldığı, bu hastaların fizik muayene ve MRI’de kanserin cerrahi olarak rezektabl olarak değerlendirildiği, ortalama yaşın 56 olduğu, ilk sistemik terapiden mCRPC safhaya geçişte ortalama sürenin 6.7 ay olduğu, mCRPC safhasından RP’ye kadar geçen ortalama sürenin de 5.1 ay olduğu, RP öncesi 5 hastanın cisplatin kombinasyonlu kemoterapi aldığı, 4 hastada RP sonrası PSA’de azalma görüldüğü, 7 hastada PSA nın RP’den sonra yükseldiği, 3 hastada ise PSA nın değişmediği, ortalama operasyon süresinin 239 dakika olduğu, ortalama kan kaybının 200 cc olduğu, 9 hastada sinir koruyucu cerrahi yapılmadığı, 1 hastada trigon rezeksiyonu sebebiyle bilateral üreteral reimplantasyon yapıldığı, PSM oranının %57 bulunduğu, patolojide 14 hastanın 12 sinde viabl kanser var olduğu ve 2 hastada hücre gurubu tarzında viabl kanser bulunduğu, RP den 1 yıl sonra 14 hastanın 12 sinin sağ olduğu, tedavi öncesi populasyonun heterojen olması sebebiyle bu girişimin faydalı olduğunun belirtilemeyeceği bildirilmiştir(237). Bu uygulamayı yapan Reichard et al nın da belirttiği gibi mCRPC’lilerde lokal tedavi olarak RP’nin yararı görülmemektedir. Reichard et al nın bu çalışması benzer başka çalışmaların bundan sonra yapılmaması açısından yararlı olmuştur.
-Metastatik kastrasyon rezistant prostat kanserlilerde (mCRPC) daha önce lokal tedavi yapılmış olmasının ilk defa uygulanacak androjen reseptör hedefli tedavilerden alınan cevaba etkisi
-Lokalize Pca’lerinde definitiv lokal tedaviler (LT) radikal prostatektomi (RP), radyoterapi RT) yada brakiterapi (BT) dir. Yakın zamanda gerçekleştirilen araştırmalarda “düşük metastatik kitleli hormona duyarlı (mHSPC)” hastalarda LT uygulamanın survival açısından yarar sağladığı bazı çalışmalarda bildirilmiştir. Definitif tedaviye rağmen bir kısım hastada nüks gelişmekte ve metastatik kastrasyon rezistant prostat kanserine (mCRPC) kadar ilerleyen progresyon görülebilmektedir. mCRPC evresinde kemoterapi ve androjen reseptör hedefli tedaviler (ARSIs yada ARAT tedaviler) uygulanır. mCRPC’li hastalar lokalize safhadayken primer lokal tedavi yapılmış olmasının mCRPC geliştiğinde sistemik tedavilere cevaba etkisi tam olarak bilinmemektedir.
–Klinik olarak gösterilmemiş olmakla birlikte preklinik çalışmalarda prostata uygulanan RT’nin “neuroendocrine” fenotip yarattığı iddia edilmiştir(238). Böyle bir sonuç androjen reseptör hedefli tedavilerle yapılan sistemik tedavilere cevabı muhtemelen azaltacaktır. Benzer olarak RP sonrası minimal rezüdüel kanser kitlesinin var olmasının sonradan uygulanacak tedavilere dirençli klonlar oluşturacağı belirtilmektedir(239). Ancak bunlar preklinik bulgulardır, bunlarla örtüşen klinik bulgular yada klinik çalışmalar henüz yoktur.
–Kastrasyon rezistant prostat kanserlilerde androjen reseptörlerini hedefleyen ajanlarla ve/veya docetaxel ile gerçekleştirilen, Japonya’dan yapılan çalışmada daha önce lokal tedavi olarak RP yapılmış olanlarda lokal tedavi almamış olanlara göre tüm sağ kalımın (OS) ve progresyonsuz sağ kalımın (PFS) daha üstün olduğu bildirilmiştir, ancak lokal tedavi olarak RT uygulanmış olanlarda bu üstünlük görülmemiştir(240). Patel et al nın retrospektif çalışmasında daha önce RP yapılmış ve post-op RT almış yada almamış mCRPC’lilerde daha önce LT yapılmamış olanlara göre daha iyi OS görüldüğü bildirilmiştir(241).
-Roy et al nın “docetaxel tedavisi almamış metastatik kastrasyon rezistant prostat kanserlilerde önceden yapılmış lokal tedavilerin (RP veya RT) ilk defa uygulanacak androjen reseptör hedefli tedavilere cevaba etkisini” araştırdıkları prospektif, randomize çalışmalarında; 1053 hastanın verilerinin değerlendirildiği, hastaların %64 nün (669 hasta) LT almış olduğu ve bu 669 hastanın %53 nün (353 hasta) LT olarak sadece RT, %16 nın (105 hasta) sadece RP, %31 nin de (211 hasta) RP + RT almış olduğu,
-ortalama takibin 49 ay olduğu, abirateron uygulananlardan LT almış vs almamışlarda ortalama radyografik progresyonsuz survival’ın (rPFS) sırayla 17 ay vs 17 ay olduğu (ns), plasebo gurubunda da LT almış vs almamışlarda rPFS’ın sırayla 8.3 ay vs 8.1 ay olduğu, abirateron vs plasebo guruplarında sırayla 349 vs 373 ölüm olduğu, abirateron gurubunda olup LT almışlarda vs almamışlarda OS’ın sırayla 37 ay vs 32 ay olduğu, plasebo gurubunda da LT almışlarda vs almamışlarda OS’ın sırayla 34 ay vs 26 ay olduğu,
-sonuç olarak analizlerde lokal tedavinin radyografik progresyon yada ölümü %13 azalttığı, abirateronun önceden LT almış vs almamışlarda rPFS vs OS yönünden anlamlı derecede farklılık yaratmadığı bildirilmiştir(242). Roy et al nın çalışmalarının sekonder analizinde abirateron’un önceden lokal tedavi almış yada almamış “docetaxel-naive” mCRPC’lilerde survival’a katkı yönünden farklılık görülmediği yada abirateronun bu iki gurup arasında anlamlı derecede survival farklılığı yaratmadığı belirtilmiştir(242). Roy et al önceden LT almış mCRPC’lilerde, özellikle RP yapılmışlarda “potansiyel olarak metastazlarında daha düşük hastalık kitlesi (kanser volümü) olduğu, sistemik tedavilerle daha iyi fonksiyonal durum olduğu ve bu sebeple kanserle ilişkili olmayan ölüm durumunun daha düşük risk taşıdığı” hipotezini ileri sürmüşlerdir.
Metastatik kastrasyon rezistant prostat kanserlerinde tedavi olarak stratejiler
-Son yıllarda metastatik kastrasyon rezistant prostat kanserlerinin (mCRPC) tedavisinde yeni opsiyonlar gelişmiştir. Bunlar; CYP17 inhibitörü olan abirateron, yeni jenerasyon androjen reseptör inhibitörleri(enzalutamid, apalutamid gibi), taxane gurubu yeni kemoterapötikler (cabazitaxel), immünoterapi (spuleucel-T), radyum-223 tedavisi gibi. Faz III çalışmalarda tüm bu tedavi seçeneklerinin sınırlı da olsa survival’a yararı olduğu gösterilmiştir. mCRPC’lerinde 2010 yılına kadar survival’a katkısı olan tek ajanın docetaxel olduğu biliniyordu(243).
-Metastatik hormona duyarlı Pca’lerinde ADT ile başlangıçta yüksek oranda cevap alınırken ortalama 1-2 yılda kastrasyon rezistant durum gelişmektedir(216,244,245). Kastrasyon rezistant durumun gelişmesinden birçok mekanizma sorumludur. Bunlar; adrenal kaynaklı androjenlerin etkisi, AR’lerinde mutasyon sebebiyle AR uyarılma yolunun(signaling) değişmesi, AR varyantlarının aktif hale gelmesi, AR gen amplifikasyonu ve aşırı üretimi(over expression) gibi. EAU guideline’ında kastrasyon rezistant durumun tarifi “serum testosteron (T) seviyesi kastre seviyedeyken (T<50 ng/dl yada 1.7 nmol/L) biyokimyasal progresyon (1 hafta aralıklarla art arda ölçümlerde nadir PSA değerinde %50 den fazla yükselmeye yol açan 3 PSA artışı) yada radyolojik progresyon gelişmesi (sintigrafide 2 yeni kemik lezyonu görülmesi yada yumuşak doku lezyonlarının büyümesi)” olarak yapılmaktadır(244). mCRPC olanlarda AR yolağı aktif durumdadır yani işlevselliğini kaybetmemiş fakat değişime uğramıştır. Bu sebeple mCRPC tedavisinde temel hedef AR sistemini etkilemek yani inhibe edebilmek olmaktadır.
–mCRPC’lilerden PSA progresyonu yada yeni semptomlar olmayanlarda görüntüleme en az yılda bir defa yapılması AUA/SUO 2023 guideline’da belirtilmektedir(220). mCRPC’li kemoterapi öncesi enzalutamid tedavisi görmüş olanlarda yapılan PREVAIL çalışmasında “PSA progresyonu olmadan hastaların %24.5 de radyolojik progresyon görüldüğü” bildirilmiştir(246). AUA/SUO 2023 guideline önerilerinde daha önce docetaxel tedavisi yada androjen reseptör hedefli tedavi almış ve hastalık progresyonu (PSA progresyonu yada radyografik progresyon yada semptomlarla ilgili yeni belirtiler) görülenlerde PSMA PET/CT sonucunda pozitif bulgu olanlarda 177 Lu-PSMA-617 tedavisi önerilmiştir.
1-Androjen biyosentezinin baskılanması
-mCRPC’lerinin tedavisinde ADT hiç kesilmemelidir. Bunun yanında androjen biosentezini etkileyen yeni ajanlar kullanılmaktadır, bunlardan biri abiraterone acetate (AA) dır,CYP17 inhibitörü olup streoidlerden androjen biyosentezini inhibe eder. FDA ve European Medicines Agency (EMA) tarfından 2011 de mCRPC’lerinde docetaxel’den sonra kullanımı kabul edilmişken 2013’de de daha önce kemoterapi uygulanmamış mCRPC’lerinde de kullanımı kabul edilmiştir(243). Daha önce kemoterapi görmüş mCRPC’lilerde plaseboya karşın abirateron’un tüm sağ kalımı anlamlı derecede uzattığı, PSA progresyonu gelişmesi süresini ve progresyonsuz survival’ı uzattığı yani PSA cevap oranını iyileştirdiği(daha yüksek oranda PSA düşüşü sağladığı)(232), kemoterapi almamış asemptomatik yada hafif semptomatik mCRPC’lilerde plaseboya karşılık radyografik progresyonsuz survival’ı anlamlı derecede uzattığı, tüm sağ kalımı anlamlı derecede uzattığı bildirilmiştir(233,247).
2-Androjen Reseptör (AR) blokajı
-İkinci jenerasyon AR antagonistleri birinci jenerasyondakilere göre daha etkilidirler. Enzalutamid bunlardan biridir, nonsteroidaldir, AR’lerine bağlanmada bicalutamid’den daha yüksek afinite gösterir, AR’lerinin nükleusa geçişini azaltır, androjen bağımlı elemanların DNA yapısını bozar, kemoterapiden sonra progresyon göstermiş mCRPC’lilerde enzalutamid kullananlarda plaseboya karşın tüm sağ kalımın anlamlı derecede daha uzun olduğu görülmüştür(234,248).
-PREVAIL çalışmasında kemoterapi almamış mCRPC’lilerde enzalutamid’in plaseboya göre radyolojik progresyonda anlamlı derecede azalma sağladığı, tüm sağ kalımda anlamlı derecede iyileşme sağladığı bildirilmiştir(249). FDA tarafından enzalutamid’in önceleri docetaxel’den sonra kullanımı kabul edilmişken bu bulgular kemoterapi almamış mCRPC’lilerde de kullanımını sağlamıştır.
-Enzalutamid yada abirateron’a rezistans primer olarak var olabilir yada sonradan gelişebilir. Bazı AR splice varyantlarının, özellikle AR-V7 var olması ikinci jenerasyon AR inhibitörlerine resistans olabileceğini göstermiştir. Diğer ikinci jenerasyon AR inhibitörleri olarak orteronel (TAK-700), seviteronel (VT-464), apalutamide (ARN-509), darolutamide (ODM-201) sayılabilir.
3-Kemoterapi
-Docetaxel: mCRPC’lerinde survival’ı uzatan ilk kemoterapötikdir, prednizon ile birlikte mCRPC’lerinde standart tedavi olarak kabul edilmektedir. Önceleri uygulanan sitotoksik bir ajan olan mitoxantrone’nun erken safhada palyasyon sağlamasına rağmen ortalama tüm sağ kalıma etkisinin docetaxel’den daha kısa olduğu gösterilmiştir. CHAARTED ve STAMPEDE çalışmalarında ADT + docetaxel vs sadece ADT uygulanmış, docetaxel gurubunda plasebo gurubuna göre tüm sağ kalımın anlamlı derecede daha uzun olduğu bildirilmiştir(182,210).
-Cabazitaxel: İkinci jenerasyon, yarı sentetik bir taxane gurubu kemoterapötikdir. Docetaxel tedavisi altındayken progresyon gösteren mCRPC’lilerde tüm sağ kalımı mitoxantrone’e karşı anlamlı derecede iyileştirdiği bildirilmiştir(243). Docetaxel, AA yada enzalutamide tedavilerinde progresyon görülen mCRPC’lilerde cabazitaxel’in antitümöral aktivesinin var olduğu belirtilmektedir(243).
4-İmmünoterapi
-Sipuleucel-T: Otolog periferal mononükleer hücrelerden oluşan Sipuleucel-T’nin asemptomatik yada minimal semptomatik mCRPC’lilerde survival’a yararı olduğu bildirilmektedir(243). FDA ve EMA tarafından 2010 ve 2013 de mCRPC tedavisinde onay verilmesine rağmen 2015 Avrupa Birliğince dağıtımı durdurulmuştur.
-Bu konuda bir diğer immünoterapi ajanı da POSTVAC-VF’dir.
-İmmün sistem stimülatörleri: Ipilimumab, nivolumab.
5-İskelet sistemi hedefli tedaviler
-Bifosfonatlar(zoledronik asit, denosumab gibi)
-Radyonüklidler (strontium-89, samarium-152, radium-223, 177 Lu-PSMA-617).
6-Genetik hedefli tedaviler ve yeni tedavi ajanları
-PARP inhibitörleri: Poly adenosine diphosphate-ribose polymerase (PARP) inhibitörlerinin mCRPC’lerinde DNA tamir defektini önledikleri, bunlardan olaparib ile olumlu cevap alınabildiği belirtilmektedir(243).
-Prostat-spesifik membran antijen (PSMA) hedefli tedaviler: PSMA Pca hücrelerinin yüzeyinden ve tümöral damarlanmalardan salgılanan bir reseptördür. PSMA işaretli (labeling) radyoizotoplarla, örneğin lutetium 177 (177 Lu-PSMA-617) yada actinum (25 Ac-PSMA-617) ile bu tür uygulamalar yapılmıştır(243).
– Sonuç olarak yeni ajanlarla survival’ı uzatmak, semptomlarda palyasyon sağlamak, hayat kalitesini iyileştirmek, komplikasyonları önlemek hedeflenmiş olmasına rağmen mCRPC’lerinde komplet cevap olmamaktadır. Radikal tedaviler uygulanmış olsun yada uygulanmamış olsun kür sağlanamamış Pca’lerinde en temel hedef kastrasyon rezistant safhaya geçişi geciktirmek olmaktadır.


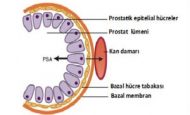



Yorumlar
Henüz yorum yapılmamış.